
|
|
|||||
|
||||||
19款兒科藥劍指新國談,獨家品種“霸屏”!摘要:
2023年至今,國家陸續出臺多項利好政策,合力驅動兒科藥創新研發。
今年以來,已有近50個兒科藥獲NMPA批準上市,其中約22個為首次獲批,集中在神經系統藥物、抗腫瘤和免疫調節劑等治療大類,涉及揚子江藥業、石四藥、恒瑞醫藥等知名藥企。
日前,2023國家醫保目錄通過形式審查名單公布,19款目錄外的兒科藥有望沖線新國談,包括5個今年獲批的新品;獨家品種為主力軍,占比接近60%。
在利好政策的全面驅動下,近年來兒科藥市場備受業內關注。
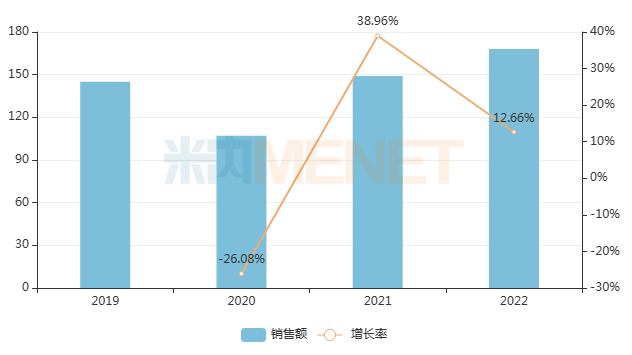
數據顯示,受疫情影響,我國兒科藥市場銷售額2020年首次出現下滑,其余年份市場銷售額增速均在10%以上,2022年銷售額再度突破1100億元,可見,兒科藥市場保持穩定增長,市場空間大。
其中,兒科中成藥在中國三大終端六大市場合計銷售規模超過168億元,同比增長12.66%。
近年來中國三大終端六大市場兒科中成藥銷售趨勢(單位:億元)
 01、22個新品強勢來襲 揚子江、石四藥、恒瑞......成績亮眼
伴隨臨床用藥需求激增,近年來兒科藥申報量、獲批量均呈現明顯上升趨勢。
2019年至今,中國已獲批的兒科藥數量超200個,且獲批數量逐年遞增,2019-2022年四年間獲批上市的兒科藥數量分別為19、26、47、66個,而今年以來已有近50個兒科藥獲批,進一步緩解兒童適宜劑型少、規格少等問題。
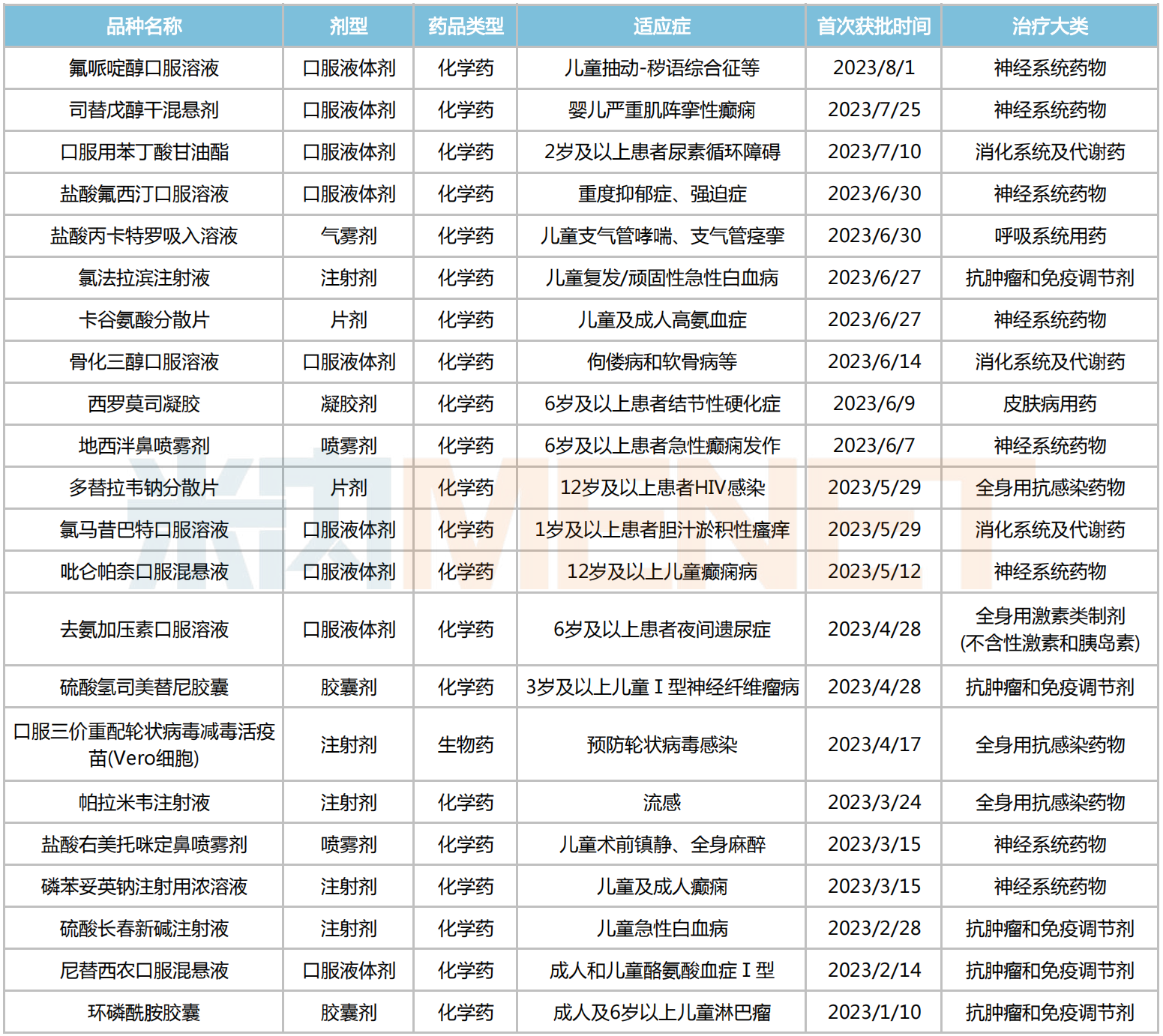
據不完全統計,近50個今年獲批的兒科藥中,約有22個品種為首次獲批上市,其中口服液體劑占比接近四成,滿足兒科用藥便利性的需求;治療大類上以神經系統藥物、抗腫瘤和免疫調節劑居多,分別有8個和5個品種進賬,消化系統及代謝藥、全身用抗感染藥物等用藥領域則各有3個新品誕生。
2023年至今首次獲批的兒科藥
 恒瑞醫藥的環磷酰胺膠囊屬于廣譜抗腫瘤藥,適用于6歲及以上兒童和成人的惡性淋巴瘤、霍奇金淋巴瘤等多種腫瘤治療;據悉,25mg的環磷酰胺口服制劑因符合兒童的生理特征和用法用量特點,在上述兒童疾病的治療中更為適用,具有明顯的臨床價值。
合肥億帆生物的氯法拉濱注射液同為兒科抗腫瘤藥,用于兒童難治性/復發性急性淋巴細胞白血病,是多年來國內少有的獲批用于兒童用白血病藥物,屬于臨床急需品種。
帕拉米韋注射液是一款主治甲流、乙流等流行性病毒感染類藥物,相較于奧司他韋等口服制劑,注射劑更便于治療無法完成自我吞咽的低齡患兒;今年以來,已有揚子江藥業、齊魯制藥、中潤藥業等6家企業的產品獲批生產,并視同過評。在此之前,本品另一制劑——帕拉米韋氯化鈉注射液已于2018年3月獲批上市,數據顯示,2022年該藥在中國公立醫療機構終端銷售額超5億元,同比增長27%。
司替戊醇干混懸劑是由石四藥開發的一款兒科罕見病藥,用于治療嬰兒期嚴重肌陣攣性癲癇綜合征(Dravet綜合征)患者全身僵直性癲癇發作。Dravet綜合征是一種罕見的難治性癲癇性腦病,已被納入2018年發布的《第一批罕見病目錄》。
02、19款兒科藥劍指新國談 獨家品種“霸屏”
為了讓更多患兒用上“質優價廉”的兒科藥,推進其加快準入醫保成為國家的重要任務之一。
日前,國家醫保局公布“2023國家醫保目錄通過形式審查名單”,390個藥品(包括348個西藥和42個中成藥)跨過國談初審“門檻”,通過藥品數創下歷史之最。
此外,新一輪國談重點繼續向罕見病藥、兒科藥等藥品傾斜,多款1類新藥、罕見病藥、鼓勵開發的兒科藥及仿制藥位列其中。
 兒科藥方面,有19個醫保目錄外藥品通過形式審查,其中化學藥15個、生物藥4個;劑型上以口服液體劑為主,有8個品種上榜;治療大類上看,神經系統藥物占據5個席位,抗腫瘤和免疫調節劑(4個)、消化系統及代謝藥(3個)、呼吸系統用藥(2個)、心腦血管系統藥物(2個)分別位居其后。
醫保目錄外通過形式審查的兒科藥
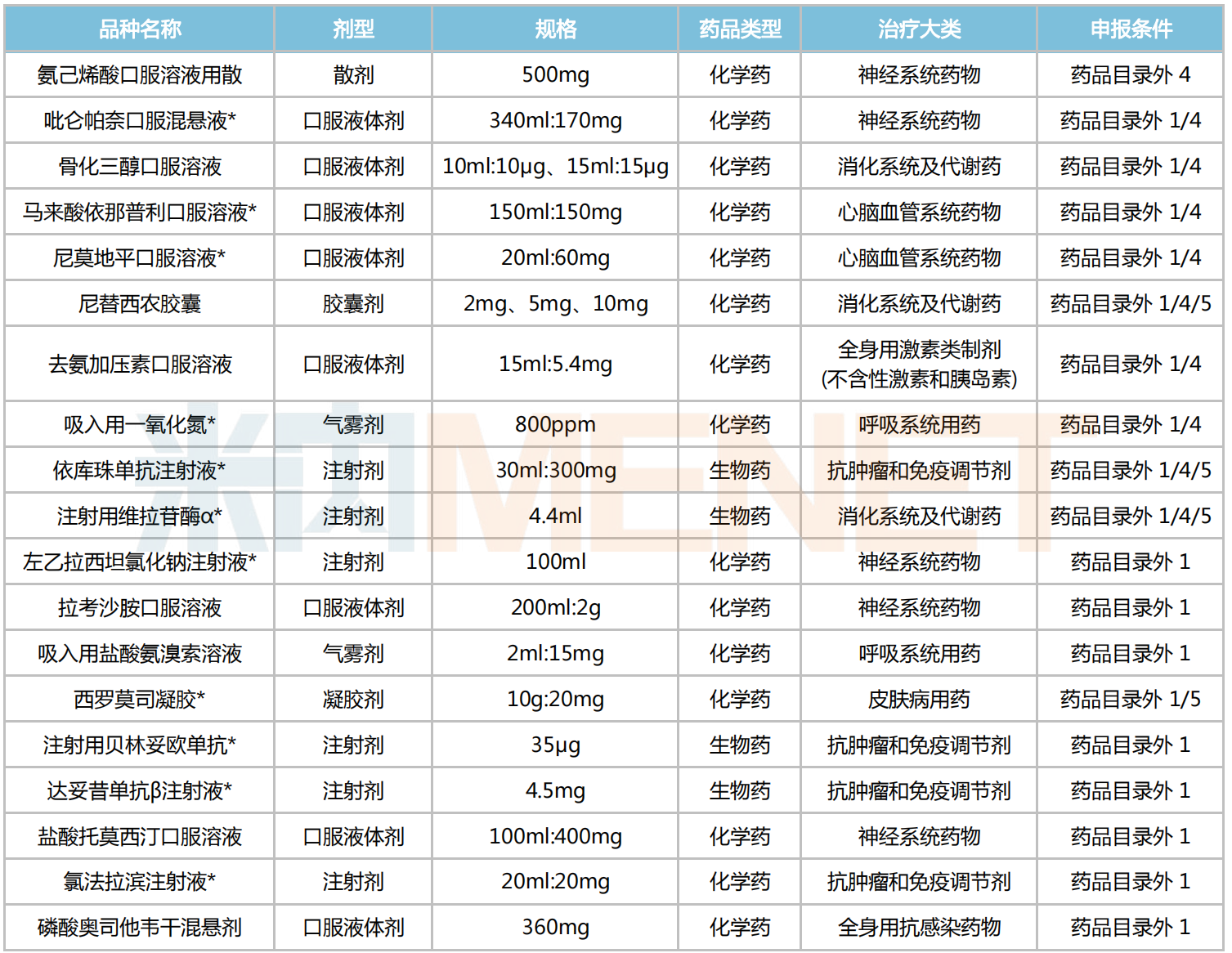 注:帶*為獨家品種
19個目錄外的兒科藥中,有5個新品在今年獲批,包括骨化三醇口服溶液、去氨加壓素口服溶液等;獨家品種占比近六成,有11個。
恒瑞醫藥的尼莫地平口服溶液用于顱內囊性動脈瘤破裂的蛛網膜下腔出血,而口服液體劑具有劑量靈活和易于吞咽等特點,尤其適用于老年人以及兒童群體,2016年該藥被納入第一批鼓勵研發申報兒科藥名單。四川百利藥業的馬來酸依那普利口服溶液為第三批鼓勵研發申報兒科藥名單品種,也是國內首個兒童專用的血管緊張素轉化酶抑制劑(ACEI)口服溶液,若該藥能順利進保,將進一步提高各年齡段高血壓、心力衰竭以及腎臟疾病患兒的用藥可及性。
吸入用一氧化氮是兆科藥業旗下的一款血管擴張劑,可用于改善脆弱新生兒群體的氧合;2020年1月,該藥被CDE以“治療兒科罕見病”為由納入優先審評,隨后于2022年3月獲批上市,是全球首款獲批的醫用NO氣體。依庫珠單抗注射液由阿斯利康開發,于2018年9月引進國內,用于治療成人/兒童陣發性睡眠性血紅蛋白尿癥(罕見病:PNH)和非典型溶血性尿毒癥綜合征(罕見病:aHUS)。武田藥品的注射用維拉苷酶α同屬兒科罕見病藥,主要用于1型戈謝病患者的長期酶替代治療;據悉,該藥在治療早期即可改善患兒的貧血、血小板減少等癥狀,并在后期持續改善或穩定其生長發育情況......
根據2023國談工作安排,通過初步形式審查的藥品將相繼進入專家審評、談判競價、公布結果及形成目錄等環節。最終,哪些藥品能成功入選,3個月后有望見分曉。
03、激勵政策層出不窮 助推兒科藥創新研發
作為特殊的用藥群體,兒童有自己獨特的生理特點,而目前兒科藥市場供應仍呈現品種少、劑型少、規格少、特藥少的“四少”現狀。另一方面,兒科藥研發生產也面臨政策法規起步晚、研發成本高、臨床試驗難推進、定價機制無明顯優勢等諸多挑戰。
對此,今年以來國家已陸續出臺多項兒科藥相關政策,合力為企業創新研發提供新思路。
2023年1月,國家衛健委發布《關于進一步加強兒童臨床用藥管理工作的通知》,鼓勵醫療機構針對兒童用藥開發可靈活調整劑量的新技術、新方法;隨后3月,國家藥監局發布《兒童抗腫瘤藥物臨床研發技術指導原則》,為兒童抗腫瘤新藥的臨床研發提供技術建議;緊接著4月,CDE發布《兒童用藥溝通交流中Ⅰ類會議申請及管理工作細則(試行)》,更好地指導和服務兒科藥研發;同年8月,國家衛健委公布《第四批鼓勵研發申報兒童藥品清單》,共涵蓋吉妥珠單抗注射劑、左甲狀腺素鈉口服溶液劑、非諾多泮注射劑等24個臨床急需兒科藥......
今年以來國家發布的鼓勵兒科藥研發相關政策
 中國是全球第二大兒科用藥市場,根據國家統計局的數據,2020年0-14歲少兒人口數為2.53億人,約占全國總人口數的18%。隨著國家“三胎”等政策全面放開,兒科用藥需求也隨之增加。預計在相關政策和用藥需求的驅動下,未來兒科藥市場將迎來巨大的發展機遇。
來源:米內網數據庫、國家醫保局等
注:上述銷售額以產品在終端的平均零售價計算。數據統計截至8月25日,如有疏漏,歡迎指正。
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|