
|
|
|||||
|
||||||
2024年53款國產1類新藥有望獲批上市(附名單)摘要:
經歷過寒冬磨礪后,中國創新藥行業的發展步伐無疑更加堅實。
2023年,是我國藥品審評審批制度改革的第八個年頭,改革紅利的持續釋放,激發起中國醫藥產業源源不斷的創新活力,我國1類新藥迎來了新的突破,33款國產1類新藥(不含預防用生物制品,下同)首次獲得國家藥監局批準上市,相比2022年(19款)大幅上漲73%,創新成績斐然。
2024年,在醫保、醫療、醫藥三大領域,政策將持續推進并創新,更多創制新藥審評審批提速。據不完全統計,恒瑞醫藥的硫酸艾瑪昔替尼片、正大天晴藥業的TQ-B3525片、海思科的HSK16149膠囊、科倫藥業的泰特利單抗注射液......53款國產1類新藥有望于今年內獲批上市。
2024年有望獲批上市的國產1類新藥(化學藥+生物藥)
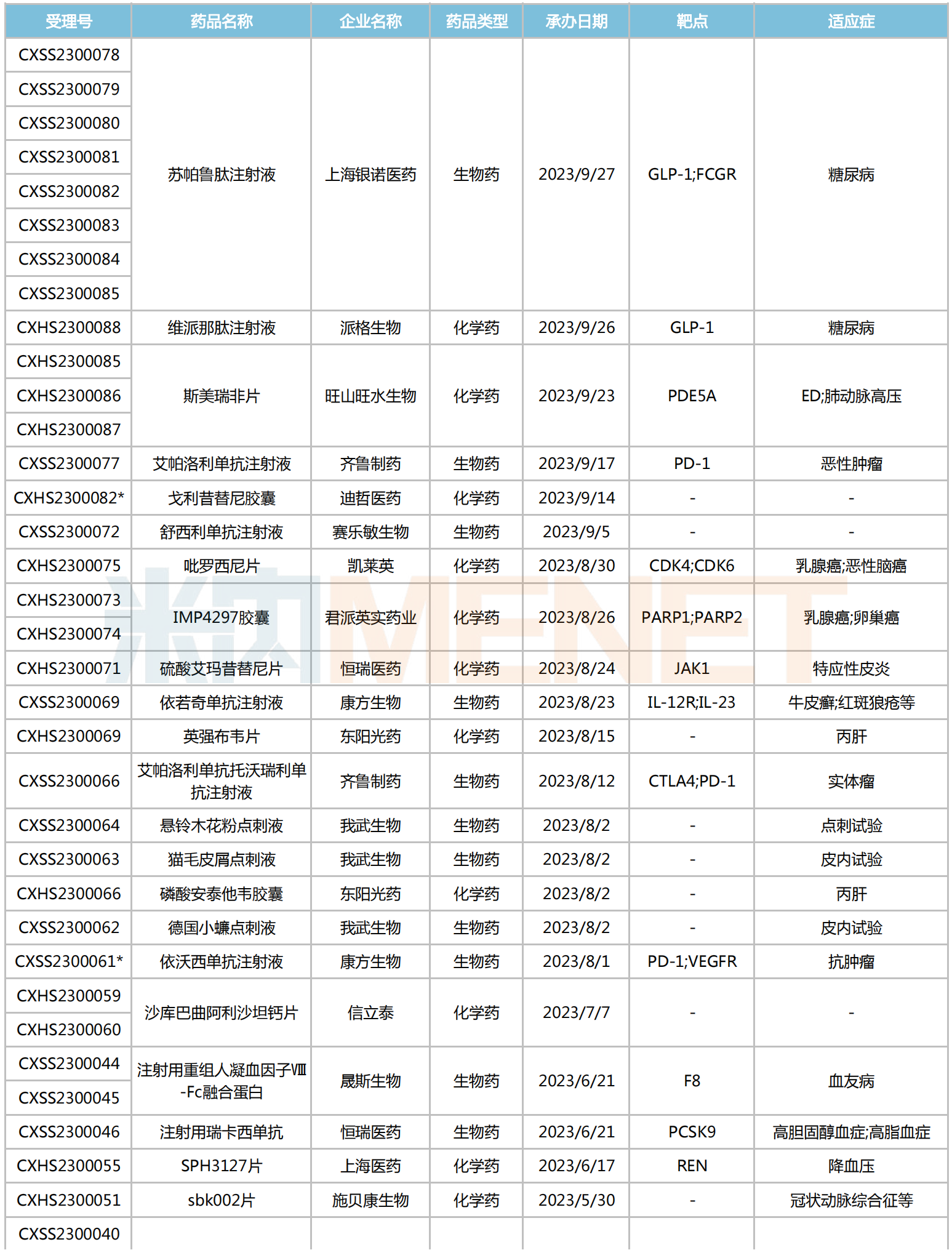 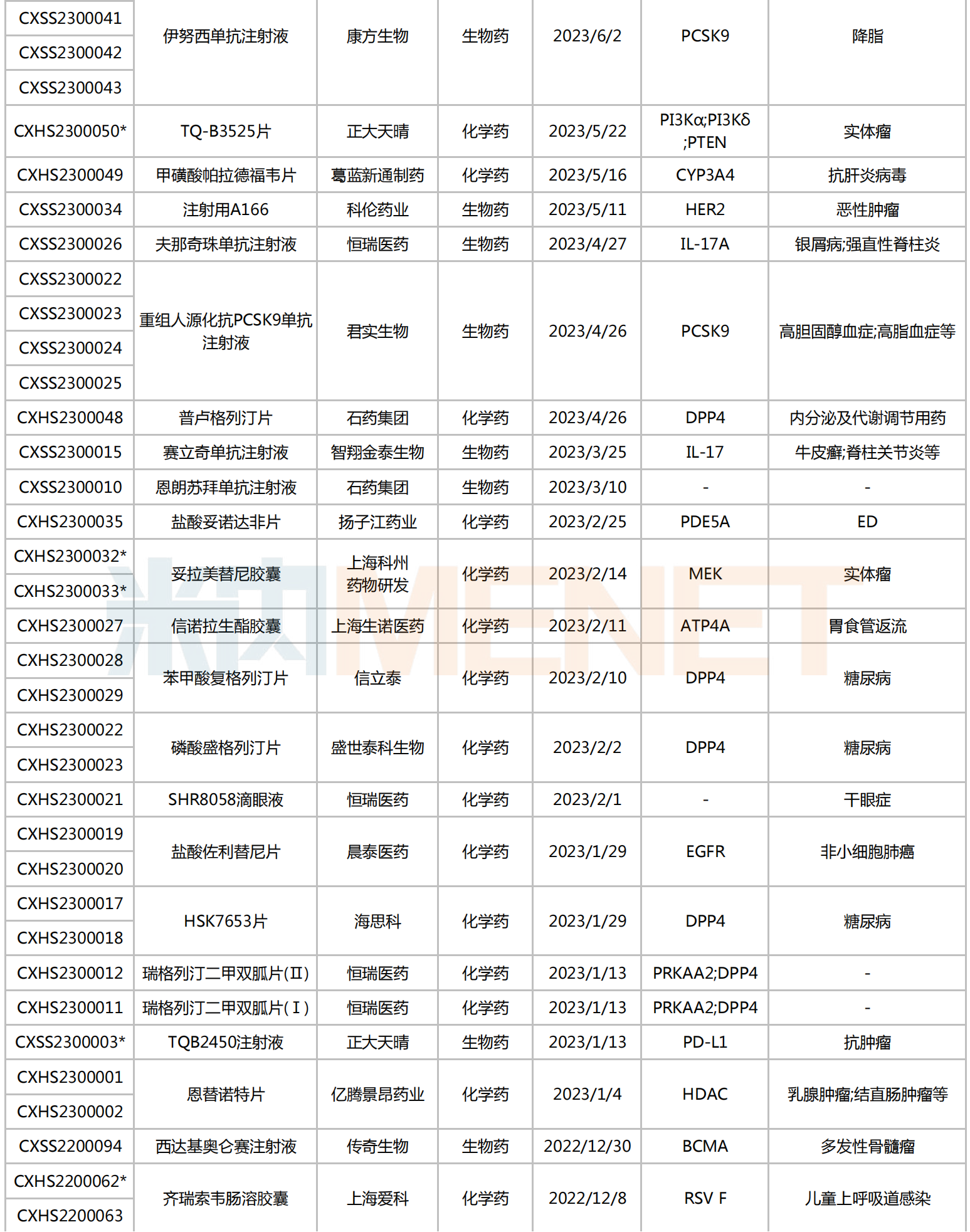 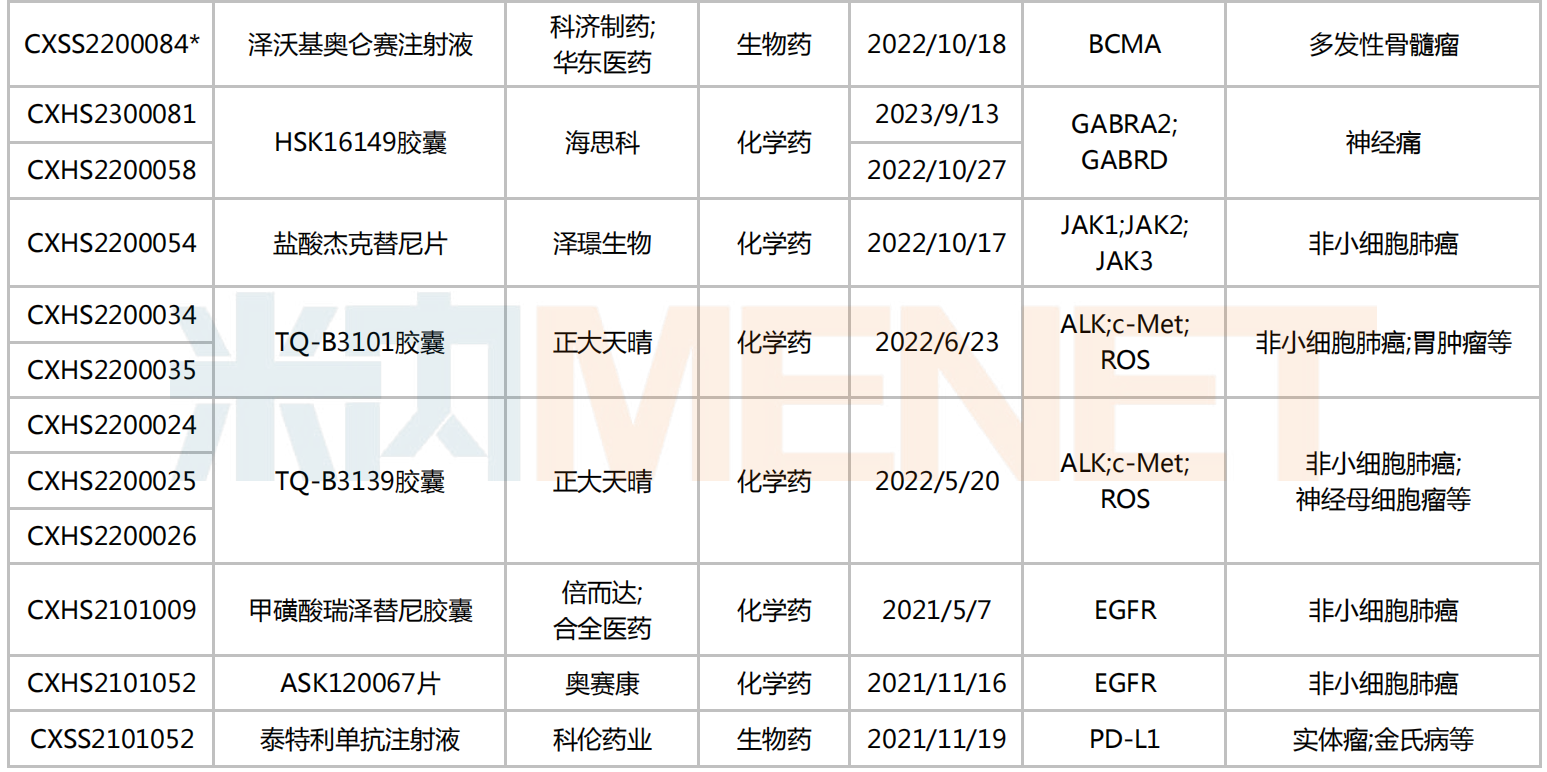 注:帶*為納入優先審評
01、恒瑞醫藥:6款1類新藥沖刺上市,首款復方降糖新品在醞釀
近年,恒瑞醫藥持續錨定創新,研發成果快速轉化落地。在研創新藥管線中,目前恒瑞有6款1類新藥進入上市沖刺期。從治療大類上看,抗腫瘤和免疫調節劑、消化系統及代謝藥居多,分別占2個席位,感覺系統藥物、心腦血管系統藥物則各占1個。
夫那奇珠單抗注射液和硫酸艾瑪昔替尼片均為抗腫瘤和免疫調節劑,其中,前者為人源化IgG1抗IL-17A單抗,適用于銀屑病、強直性脊柱炎等,其對標產品——諾華的司庫奇尤單抗2022年在中國公立醫療機構終端銷售額超14億元;后者為新一代高選擇性JAK1抑制劑,適用于治療中至重度特應性皮炎,目前尚未有國內企業自研的JAK1抑制劑獲批上市。
近年來中國公立醫療機構終端司庫奇尤單抗銷售趨勢(單位:萬元)
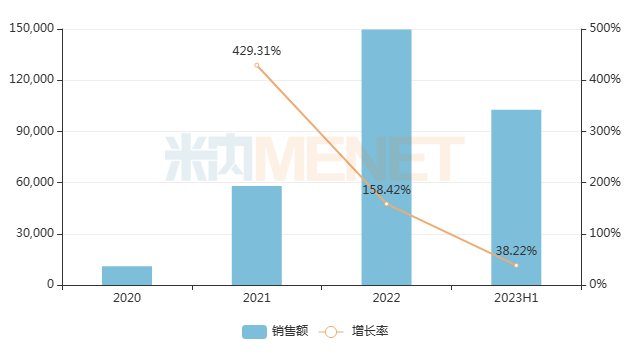 瑞格列汀二甲雙胍片(Ⅰ)/(Ⅱ)均為創新DPP-4抑制劑復方降糖藥,可通過兩種不同作用機制達到降糖作用,且固定劑量復方制劑能減少藥物漏服,以及提高治療依存性。若后續瑞格列汀二甲雙胍順利獲批上市,將成為首款國產口服降糖藥復方1類新藥。
此外,SHR8058滴眼液是從Novaliq公司引進的干眼癥新藥,目前國內暫無同類產品獲批上市;注射用瑞卡西單抗是一款抗PCSK9單抗,臨床結果顯示,該藥聯合他汀類藥治療高膽固醇血癥患者,給藥間隔時長可達12周(已上市的PCSK9抑制劑給藥間隔為2周或4周)。
02、正大天晴:4款抗腫瘤新藥穩步推進,10億明星藥競品蓄勢待發
作為國內創新藥龍頭企業,正大天晴藥業聚焦打造領先的抗腫瘤新藥產品線,4款抗腫瘤1類新藥有望在今年獲批上市,包括3款小分子化學藥和1款大分子生物藥。
其中,TQ-B3525片是一種新型的PI3Kδ/α雙重抑制劑,于2021年7月獲準納入突破性療法審評程序,擬用于既往至少二線治療失敗的復發/難治濾泡性淋巴瘤的治療,這是其斬獲的首個突破性療法;TQ-B3139膠囊是新一代ALK抑制劑,對標克唑替尼,在中國公立醫療機構終端,克唑替尼2020年的銷售規模已超過10億元。
近年來正大天晴藥業納入突破性療法品種情況
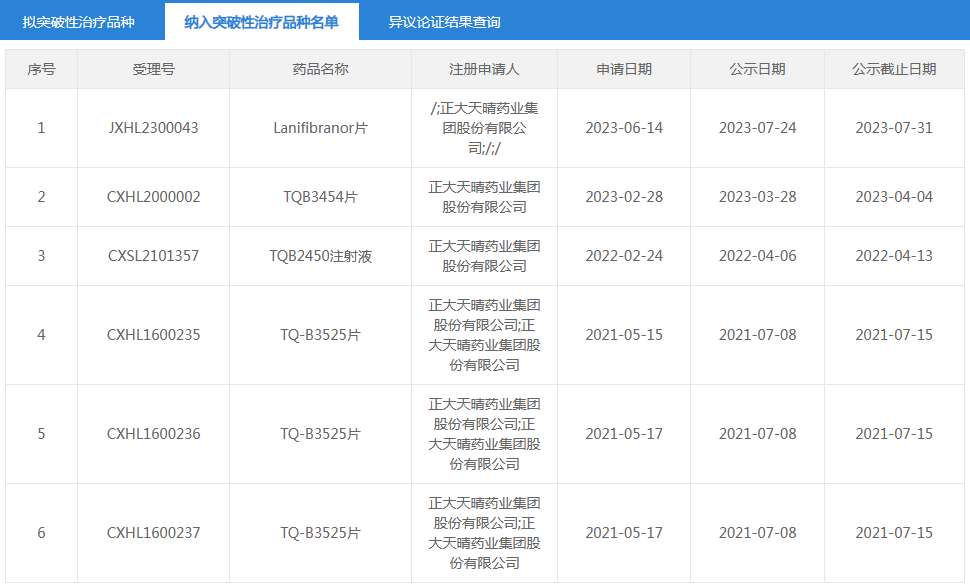 來源:CDE官網
TQ-B3101膠囊屬于ROS1/ALK/c-Met抑制劑,可選擇性地抑制ROS1陽性、ALK陽性和c-Met腫瘤細胞的體外增殖,對非小細胞肺癌的療效甚佳,且眼部毒性低、安全性良好;TQB2450注射液是一款人源化PD-L1單抗,目前已在國內開展多項頭對頭臨床試驗,2024年1月,該藥被納入優先審評品種名單,擬用于聯合鹽酸安羅替尼膠囊治療復發性/轉移性子宮內膜癌。
TQB2450注射液已進入Ⅲ期臨床的適應癥
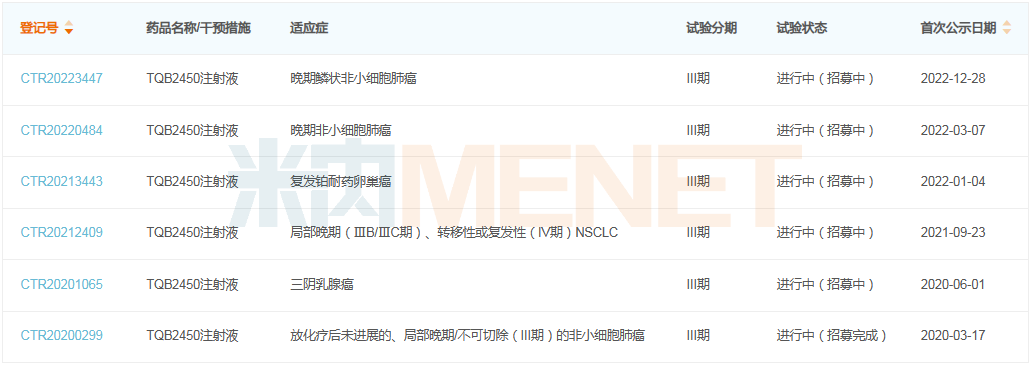 03、科倫藥業:對標$24億明星藥,其首款HER2 ADC上市可期
自2012年轉型至今,科倫藥業已成功實現了從單純大輸液到全面、綜合、內涵發展的蛻變。與此同時,其積極推動變革,創新研發進一步提速。
泰特利單抗注射液于2017年9月首次獲批臨床,2021年11月首次提交上市申請,是科倫首個申報上市的1類新藥,也是全球首個針對鼻咽癌適應癥提交NDA的PD-L1單抗。
泰特利單抗注射液項目進度情況
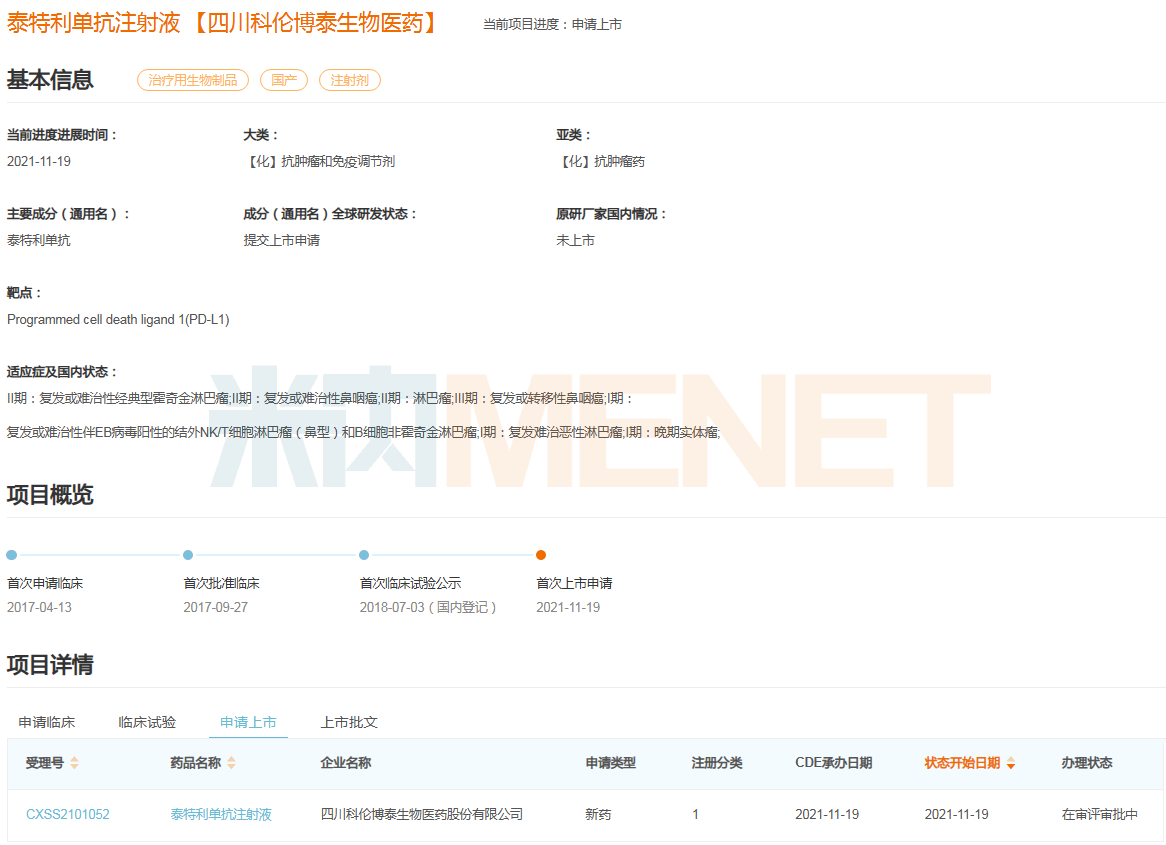 注射用A166為科倫首個申報上市的靶向HER2 ADC,兼具抗體藥物的靶向性以及化療藥物的高殺傷性等特點,是其首個中美臨床研究項目。該藥對標產品為羅氏的恩美曲妥珠單抗。數據顯示,2022年恩美曲妥珠單抗全球銷售額超24億美元(按實時匯率換算)。
恩美曲妥珠單抗全球銷售趨勢(單位:億美元)
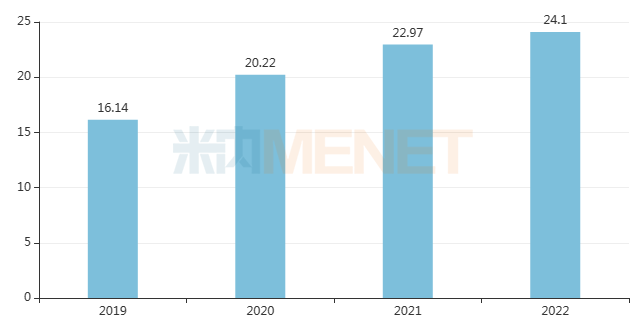 04、海思科:發力降糖領域,全球首款DPP-4雙周制劑獲批在望
近年來,海思科以“創新”為內核,不斷加大研發投入力度,2023年前三季度研發費用3.42億元,同比增長23.19%。深耕創新藥多年,其創新藥管線逐步迎來兌現期。
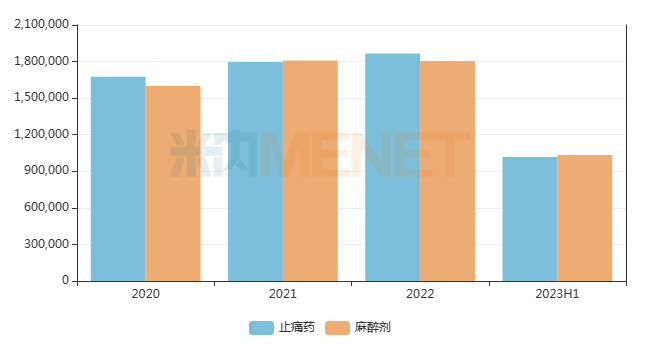
其中,HSK16149膠囊是一款口服γ-氨基丁酸(GABA)類似物,屬于普瑞巴林的me-better藥物,具備高靶點選擇性、強效鎮痛、長效鎮痛、中樞副作用小等特點,已報產適應癥包括糖尿病周圍神經痛、帶狀皰疹后神經痛。麻醉鎮痛是海思科重點布局的治療領域,2022年中國公立醫療機構終端麻醉劑及止痛藥合計銷售規模超過360億元。
中國公立醫療機構終端麻醉劑及止痛藥銷售趨勢(單位:萬元)
 HSK7653片是一款長效DPP-4抑制劑,用于治療2型糖尿病。在糖尿病用藥領域,海思科目前僅有1款仿制藥格列齊特緩釋片獲批上市,HSK7653片是其在該領域首款申報上市的1類新藥,若該藥能成功獲批,將成為全球首個上市的DPP-4雙周制劑。
2022年以來海思科申報上市的糖尿病用藥
 05、東陽光藥:狙擊1500億市場,2款抗感染1類新藥在路上
創新轉型已成為東陽光藥近年來發展的主旋律,特別在抗感染領域,其首款1類新藥磷酸依米他韋膠囊已于2020年12月獲批上市,成為國內首款自主研發的抗丙肝口服小分子新藥;10款主要在研1類新藥相繼步入臨床及申報上市階段,涉及丙肝、乙肝、流感等疾病。
東陽光藥抗感染新藥研發管線
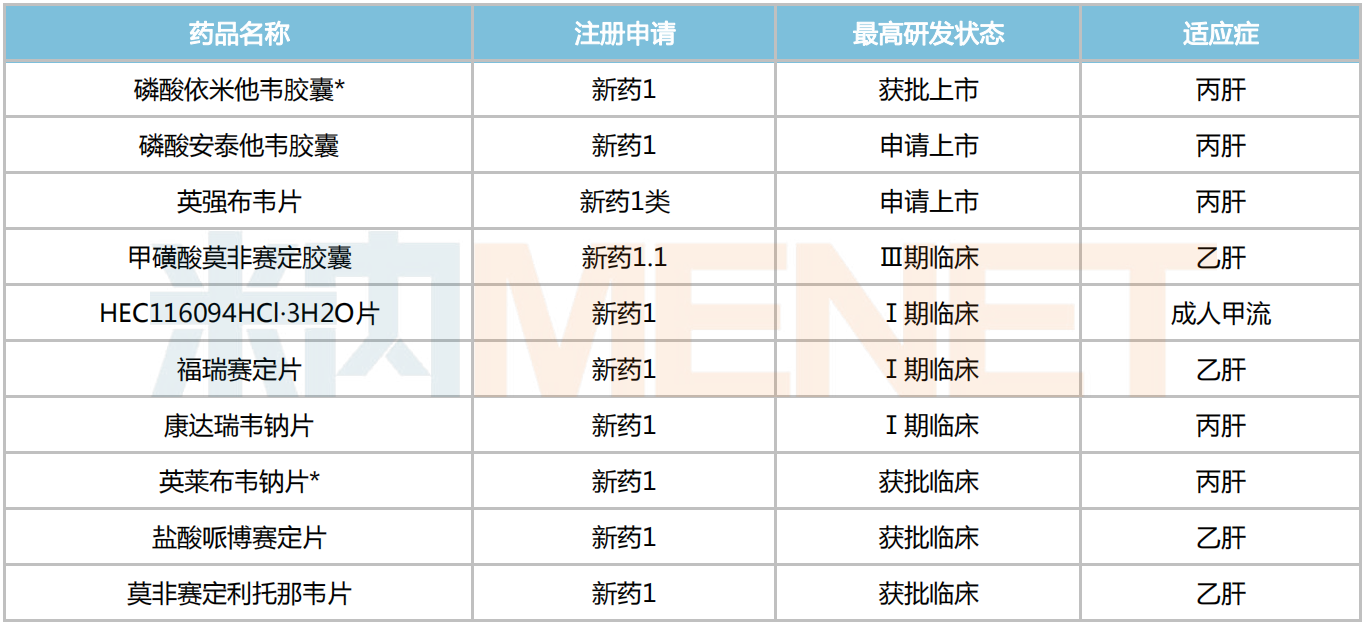 注:帶*為納入優先審評品種
其中,2款抗丙肝病毒1類新藥——磷酸安泰他韋膠囊、英強布韋片的上市申請均于2023年8月獲得CDE承辦,最快有望于2024年內獲批上市。據東陽光藥表示,其正開發磷酸安泰他韋膠囊聯合英強布韋片用于丙肝的治療。
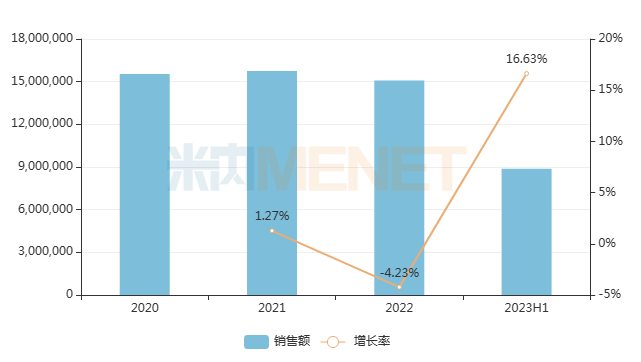
數據顯示,2022年中國公立醫療機構終端全身用抗感染藥物銷售規模超1500億元,2023年上半年已超過880億元,同比增長16.63%,全年有望再創佳績。
近年來中國公立醫療機構終端全身用抗感染藥物銷售趨勢(單位:萬元)
 06、結語
自2015年《藥品注冊管理辦法(修改草案)》的提出,創制的新藥、治療疑難危重疾病的新藥等特殊審批流程得到進一步優化。改革的啟動,讓創新藥產業的崛起迎來了契機。時至今日,我國本土醫藥創新已走過初期“野蠻生長”的階段,正迎來“大浪淘沙”的發展階段,真正具有臨床價值的創新藥將會被留下。
來源:米內網數據庫、CDE官網
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|