
|
|
|||||
|
||||||
仿制藥一致性評價現狀、問題及建議報告解讀摘要:
醫藥網10月16日訊 我國是一個發展中國家,同時也是個仿制藥大國,國內企業生產的化學藥產品絕大多數為仿制藥。為了根本性地提升我國仿制藥質量,從2012年開始,國家藥監部門提出了仿制藥質量和療效一致性評價(以下簡稱“一致性評價”)的系統性工程。
為了讓社會更好的理解一致性評價工作,推進中國仿制藥產業全方位轉型升級,一致性評價在行動組織與E藥經理人一起合作,對我國仿制藥行業的發展和一致性評價相關的行業政策進行了深入研究并形成了《仿制藥質量與療效一致性評價現狀、問題及建議》報告。
 《仿制藥質量與療效一致性評價現狀、問題及建議》報告主要內容:
 第一章:全球及中國仿制藥行業現狀
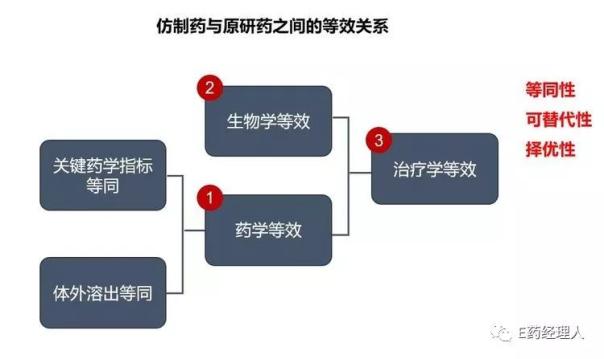
仿制藥的本質在于“等效和可替代”
仿制藥是醫藥市場的重要組成部分,雖然各國對仿制藥定義的具體表述不同,但與原研藥在質量與藥效上具有等同性,并在臨床上可替代,是全球對仿制藥的普遍訴求。
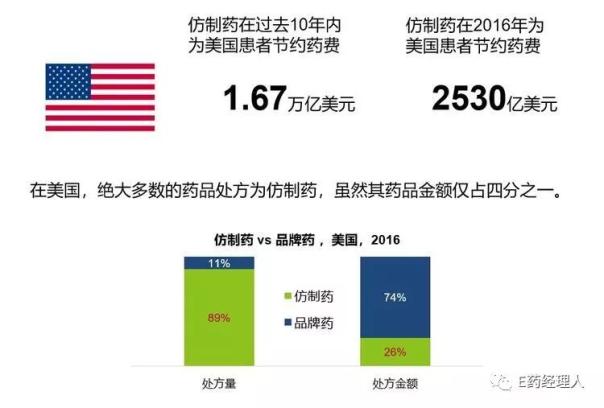
 仿制藥替代專利過期原研藥物是全球性趨勢
與原研藥相比,仿制藥的研發投入相對較低且無需高風險、高成本的臨床研究,因此價格較低。這也意味著在醫療成本持續增長的當前,仿制藥替代原研藥成為全球的大勢所趨。
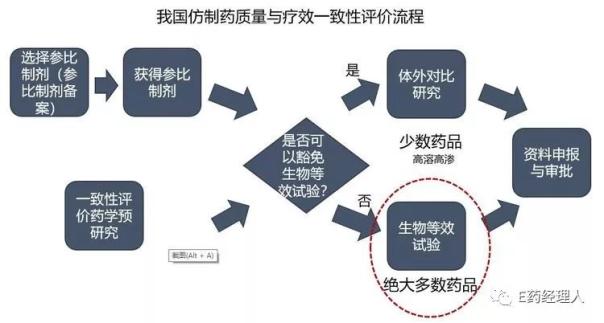
 第二章:中國仿制藥一致性評價方法及進展
我國的一致性評價工作遵循了包括美國在內的國際上大多數國家的做法,讓仿制藥與參比制劑進行人體體內的生物等效性實驗。這一做法不僅順應國際主流標準,而且提升了我國仿制藥等效性研究的標準,同時加大了我國一致性評價的難度和企業的研發投入。
 通過政府和企業的共同努力,一致性評價工作初顯成效:
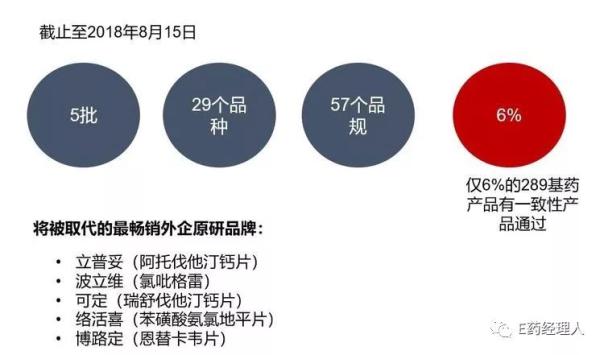 第三章:中國一致性仿制藥市場及現狀分析
國家制定了一系列的政策鼓勵仿制藥盡快通過一致性評價,旨在通過評價品種的市場準入,逐步限制直至淘汰未通過的品種,為通過一致性評價的仿制藥創造條件提供與原研相同的待遇。
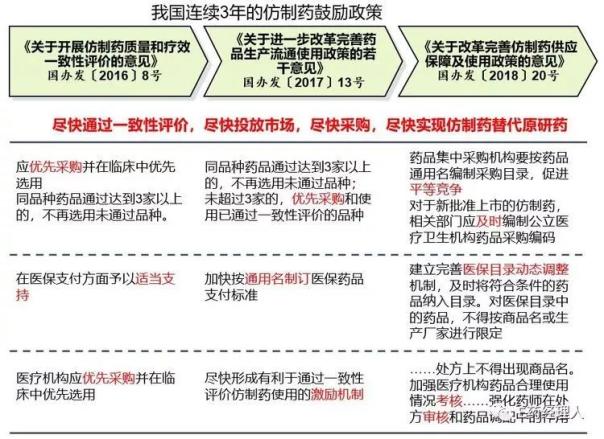 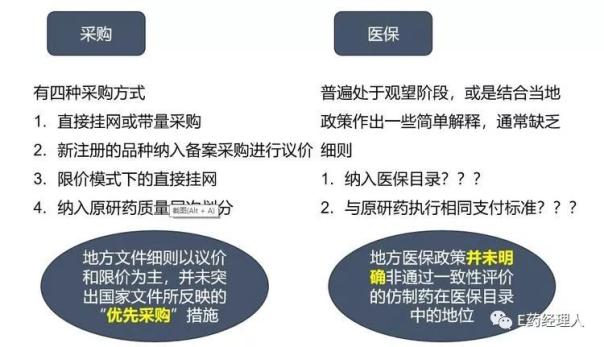 另外,市場中的某些管控政策對一致性仿制藥的普及也產生了不利影響,如果各省市在政策制定的過程中能更多考慮到促進消除高質量一致性仿制藥市場準入的一些壁壘,這些地方政策也將更能產生有益的政策效果,促進高質量一致性仿制藥對原研產品的替代:
 第四章:中國一致性評價工作的問題及建議
醫生、患者及監管者對一致性評價的認知是影響一致性仿制藥替代原研藥的重要因素,但通過對醫生的訪談調查發現醫生對一致性仿制藥的認知仍不清晰:
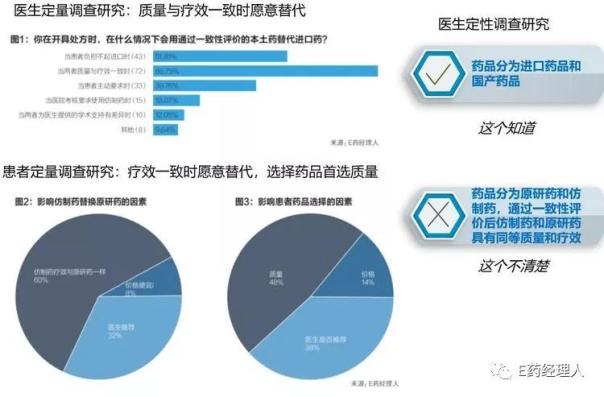 基于此,本報告也提出了推進一致性評價的相關建議:
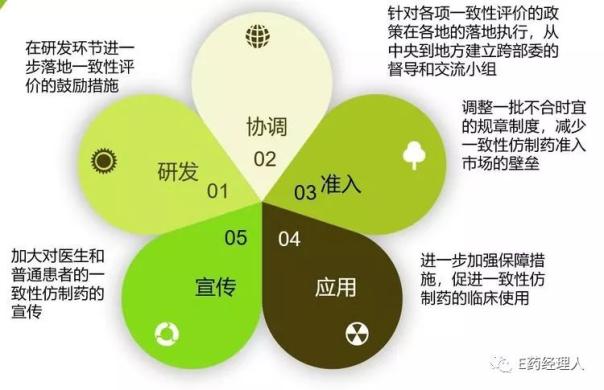 |
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|