
|
|
|||||
|
||||||
國家藥監局開出開年首張“境外罰單”摘要:
醫藥網1月22日訊 1月18日,國家藥監局公布《5家進口醫療器械境外生產現場檢查結果》。其中明確:
對5家外資企業執行中國醫療器械生產質量管理規范存在的問題,國家藥品監督管理局已要求企業落實整改措施并提交整改報告。
BD等5家外資巨頭械企遭查
也就是說整個2018年,國家藥監局對9個國家的26家進口醫療器械生產企業行了境外生產現場檢查!且5家外資巨頭械企本次被通報整改!
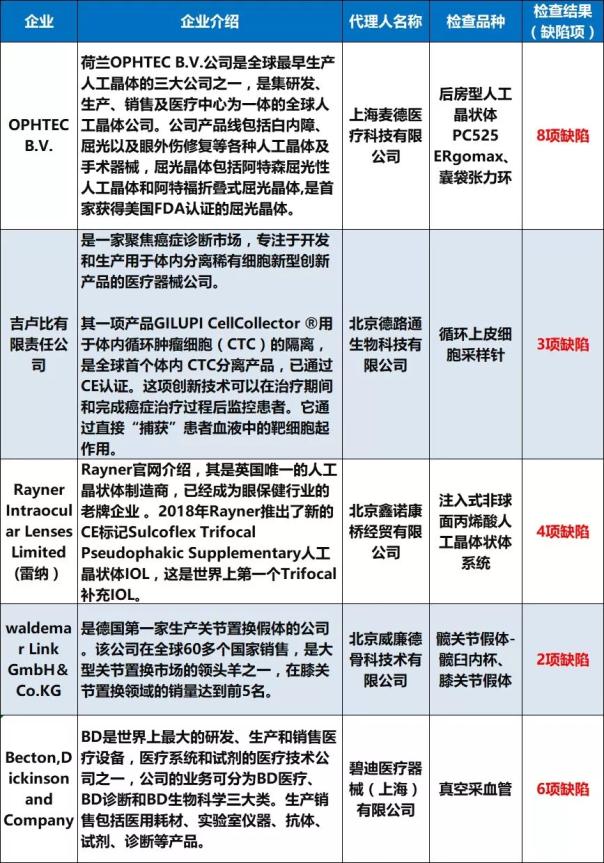
被通報整改的5家外資巨頭械企,包括BD、Rayner(雷納)等全球醫療器械巨頭企業!在單個或多個產品檢查中,均被查出缺陷,沒有一家是零缺陷!
被查出缺陷的醫療器械產品,包括人工晶狀體、囊袋張力環、循環上皮細胞采樣針、關節假體、采血管等。
 國家藥監局
醫療器械境外檢查力度越來越大
截止到2018年底,國家局已對71家境外醫療器械生產企業展開了現場檢查。其中29家企業的檢查結果已在官網通報。
早在2015年,藥監總局就啟動了對境外醫療器械生產企業的生產現場檢查工作,強生和美敦力這兩家全球醫療器械行業排名前兩位的企業,被選擇作為檢查對象。
接著:
 而從本次發布的公告結果可知,2018年對境外械企的生產現場檢查已經達到26家!境外檢查力度越來越大!
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|