
|
|
|||||
|
||||||
全國輔助用藥目錄出臺在即 專家諫言藥企轉型策略摘要:
醫藥網1月24日訊 2018年12月,國家衛健委發布《關于做好輔助用藥臨床應用管理有關工作的通知》(下稱《通知》),紅頭文件傳達的一個重要信號是,國家版《輔助用藥目錄》即將出臺。這一政策導向再次將本就被重點監控的輔助用藥推至風口浪尖。
“從全國來看,國家版輔助用藥目錄的出臺,將有效控制輔助用藥濫用的現象,部分輔助用藥將被停用。”北京醫院藥劑科主任胡欣表示,國家政策以患者利益為出發點,不會出現因此影響臨床治療效果、患者用藥需求的問題。
重壓之下,醫療機構加緊重點監控臨床輔助用藥的步伐;依靠生產、銷售輔助用藥的藥企或裁員,或轉型;患者使用輔助用藥自付部分或將提高,亦或面臨“買不到藥”的境況。
遴選不可“一刀切”
根據《通知》,各地衛生健康部門于2018年12月31日前將匯總的輔助用藥目錄上報至國家衛健委。國家層面明確截止時間之后,海南、河北、安徽、廣東等地紛紛下發文件,要求本地醫療機構上報輔助用藥目錄。
以河北省為例,該省要求醫療機構按照年度使用金額,以通用名稱對其由多到少進行排序,形成輔助用藥目錄,報送品種不少于20個。健康界從河北醫科大學第三醫院獲悉,該院已在規定時間內完成上報工作,上報品種主要集中在中藥注射劑等方面。
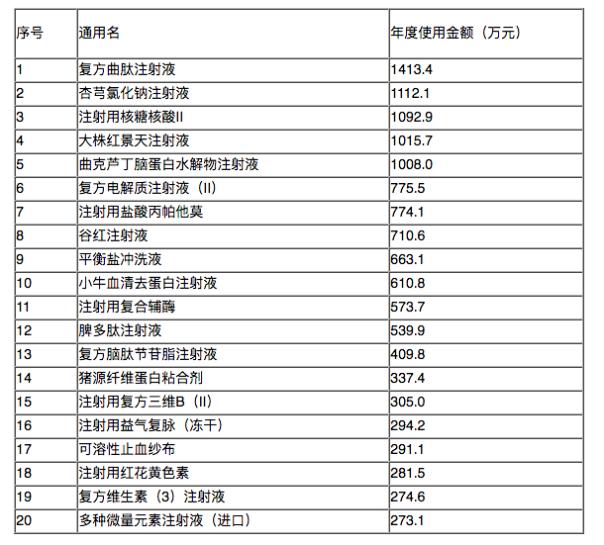 數據來自河北醫科大學第三醫院
胡欣告訴健康界,收到國家衛健委《通知》后,北京醫院亦按照相關要求完成了輔助用藥目錄申報工作。
胡欣介紹了北京醫院挑選輔助用藥時遵循的幾個原則:1)醫院用藥金額排名前100的;2)沒有指南推薦的;3)臨床證據不充分的;4)適用于多種疾病的;5)中國藥典沒有收載的。總體來看,那些又貴又不好用的“萬金油”未來被“踢出局”的可能性很大。
遴選輔助用藥,首都醫科大學附屬北京中醫醫院特地制定了評選活動,登錄評選界面,網友可以在一系列輔助用藥列表中選擇20種藥品。
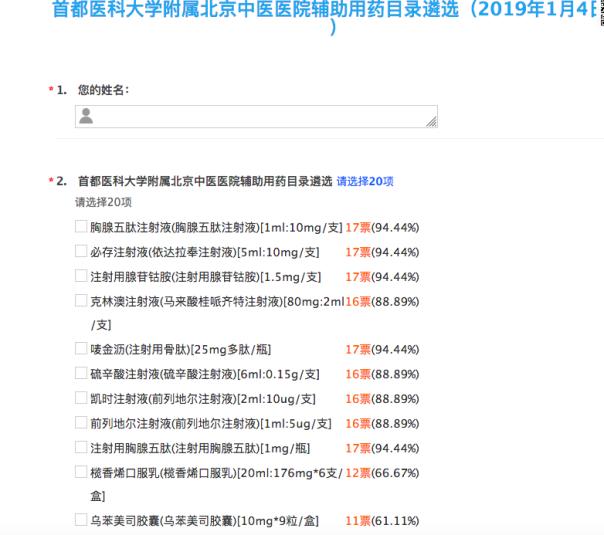 《通知》出臺之后,“按照藥品使用金額排序確定輔助用藥目錄”的評價標準被視為“一刀切”的做法。部分反對派認為,這一做法或致部分具有臨床價值的輔助用藥“蒙冤”。
對此,國家衛健委衛生發展研究中心衛生技術評估室副研究員劉躍華于近日表示,國家出臺輔助用藥目錄的初衷是引導合理使用藥品,同時肯定合理使用輔助用藥對于緩解患者治療不良反應等方面的作用。“國家真正管的是超適應癥、超劑量、超療程等不合理使用的情況,不會一下子拍死。”
政策影響出現但還未最大化
其實,早在《通知》出臺前,部分省市已經出臺了輔助用藥目錄,醫療機構輔助用藥使用亦被重點監控,但國家版輔助用藥目錄即將出臺的趨勢仍對各方產生影響。
“長久以來,我國的確存在部分輔助用藥濫用的情況。”胡欣告訴健康界,例如,部分輔助用藥使用金額超過腫瘤靶向藥物用藥金額,一旦出現這種情況,醫院必須采取限用或停用舉措。
早在2017年,北京市印發《關于加強醫療機構重點監控藥品管理的通知》,要求醫療機構將非治療必須、臨床療效證據不充分的藥品列為“重點監控藥品”,各醫療機構建立相關目錄,連續3個月進入醫療機構銷售前20位的重點監控藥品,采取限用或停用等舉措。
這一文件對于輔助用藥的監控,與國家版《通知》大體相同。由于醫保基金持續吃緊,以三明市為代表的諸多省市早已向輔助用藥開刀。毫無意外,2018年的醫藥改革對藥企產生了較大影響。
華潤三九2018年半年度報告顯示,由于輔助用藥目錄政策等壓力,中藥注射制劑等非臨床一線用藥品種的銷售和推廣面臨困難。昆藥集團2018年半年度報告同樣顯示,由于公司主導藥品品種被列入限制二級以上醫院使用的范圍,其銷售量下降26%左右。
對藥企來說,藥品銷售量下降無疑讓部分從業者雪上加霜。受輔助用藥政策、藥品集中采購等政策影響,不少藥企邁出裁員這一步。2019年初,輝瑞宣布關閉位于印度的兩家非專利注射液生產工廠,這一決定或將導致1700多名員工失業;2019年1月8日,美國制藥公司禮來宣布裁撤250個工作崗位;宣布裁員的還有阿斯利康等老牌藥企。
一位負責中藥注射液銷售的醫藥代表告訴健康界,與前些年相比,銷售額已出現明顯下降趨勢,不少醫藥代表不得不轉行。近日,江西省一位醫藥代表向媒體反映,該區域原本有80多位銷售人員,一年下來,已經“走了”一半多。
即便哀鴻遍野,以輔助用藥為代表的醫藥領域改革仍然會向縱深推進。劉躍華預言,2019年醫藥改革中,輔助用藥應該首當其沖,是第一個要整頓的領域。
醫院重點監控 藥企尋求轉型
政策重壓下,醫院多措并舉監控輔助用藥,藥企紛紛尋求轉型之路。
——醫院重點監控
胡欣表示,為了控制輔助用藥濫用現象,北京醫院在科學分析的基礎上,對部分輔助用藥限制用藥科室,限制開藥醫生級別,限制用藥病種。此外,部分醫院還通過信息化系統,實現以上舉措。有些醫院的做法是,將科室輔助用藥使用情況與績效考核掛鉤。
限制輔助用藥使用,國家衛健委要求醫療機構要根據臨床診療實際需求,制訂本機構輔助用藥臨床應用技術規范,明確限定輔助用藥臨床應用的條件和原則,要求醫師嚴格掌握用藥指征,嚴格按照藥品說明書使用,不得隨意擴大用藥適應證、改變用藥療程、劑量等。
與此同時,醫療機構要進一步加強臨床路徑管理,科學設計臨床路徑,規范臨床診療行為;對輔助用藥管理目錄中的全部藥品進行重點監控;嚴格落實處方審核和處方點評制度,將輔助用藥全部納入審核和點評范疇,充分發揮藥師在輔助用藥管理和臨床用藥指導方面的作用。
——藥企尋求轉型
通常而言,藥品之所以被列入輔助用藥或被重點監控,其原因大體為藥物治療效果不確切、藥理機制不明且非對癥治療性藥物。部分藥品即便原先為治療性藥物,但由于更新換代慢等原因,同樣可能淪為輔助用藥。
國家限制輔助用藥高壓下,企業還需“打鐵自身硬”。在轉型之路上,“賽柏藍特約撰稿人燁華”撰文建議,企業要加強藥品篩選和產品線梳理;加強藥品研發投入并提升藥品質量;加強臨床療效研究,力爭使藥品適應癥明確;加強進入臨床路徑及疾病治療指南的工作,減少淪為輔助用藥的機會。
劉躍華建議,未來,輔助用藥在臨床路徑中找到自身的獨特價值是重點。以中藥注射劑為代表,部分輔助用藥可以尋找現有藥物開展聯合用藥,亦或將部分注射劑產品改變用藥路徑,變為口服劑型。
劉躍華表示,從支付角度出發,企業或者醫療機構可以找到更多支付方,例如將商業保險與某一種治療藥物進行捆綁等,亦不失為是一種短暫策略。
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|