
|
|
|||||
|
||||||
在進口替代大背景下 國產血管介入耗材如何提高市場話語權?摘要:
醫藥網11月26日訊 2019年,國產高值耗材迎來巨變。從“兩票制”到“高值耗材集中采購”,高值耗材的銷售渠道與銷售方式不再與以往相同;從仿制產品到自主創新,國內高值耗材正在不斷優化;從進口為主向國產化發展,國產高值耗材相關企業迎來不同的境遇……
過去四個月的時間,據不完全統計,動脈網報道了32個相關企業,多名心外科專家,聯合中國醫藥教育協會心臟外科專業委員會、中國醫藥生物技術協會心血管外科技術與工程分會發起“從心出發——2019中國十大心血管技術創新案例征集活動”,并承辦“FTC2019中國心臟外科前沿技術論壇”。
在此過程中,我們發現2019年高值耗材領域有以下變化:
1、資本整體趨冷但仍舊熱衷有核心競爭力的醫療企業;
2、高值耗材市場仍在不斷擴張;
3、高值耗材企業的銷售模式正在轉變,經銷商面臨挑戰;
4、國內高值耗材企業正在不斷創新,產品陸續獲批或進入綠色通道,國際品牌將接受挑戰;
5、創新企業迎來發展契機,同質化企業將逐漸淘汰;
6、越來越多的高值耗材領域企業開始探尋國產化道路。
鑒于大家對高值耗材如何提高市場話語權十分重視,動脈網結合2019年血管介入領域企業的發展與政策的演變,試圖回答這個問題。
2019資本回顧
醫用高值耗材領域,2019年的資本大事件莫過于啟明醫療赴港上市(11月10日,港交所披露啟明醫療通過聆訊后的招股書)。其他創新企業也多有融資,脈搏醫療、唯柯醫療、心瑋醫療、麥普奇醫療、上海百心安、脈全醫療、沛嘉醫療、健世生物、蘇州同心醫療等企業在2019年完成新一輪融資,融資金額從千萬元到億元不等。
事實上,盡管今年(2019)資本市場遇冷,投資機構對于資金更加謹慎,但是對于醫療產業而言,資本投資仍舊熱情。其中不乏政策轉好、企業創新等因素。
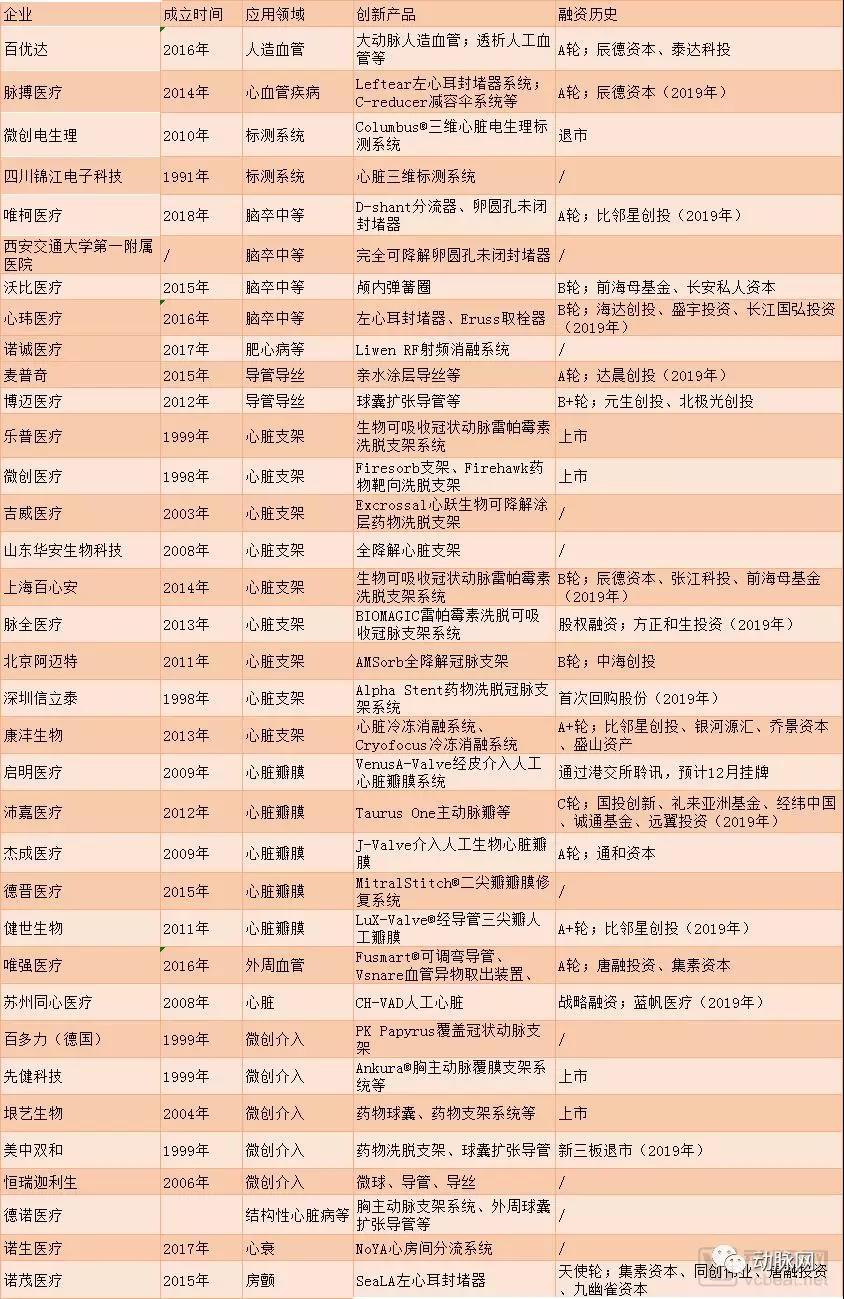 (不完全統計,心血管介入耗材領域企業情況)
2014年2月7日,國家食品藥品監督管理總局發布了《創新醫療器械特別審批程序(試行)》(食藥監械管〔2014〕13號),自2014年3月1日起施行。該程序是在確保上市產品安全、有效的前提下,針對創新醫療器械設置的審批通道。
按照該程序,對于創新型的醫療器械注冊,省局20個工作日初審,其后國家局40個工作日內必須出具審查意見。如果一切順利,創新產品僅需60個工作日即可進入公示期,公示期最短為10個工作日。總體而言,從申報到注冊完畢,有可能15周左右完成,與以往的審批時間相比大大縮減,尤其是針對需上報國家局審批的三類境內產品,企業將可更快獲批上市。
《創新醫療器械特別審批程序》實施以來,加速推進了創新性強、技術含量高、臨床需求迫切的醫療器械產品上市,同時加快了高端醫療器械國產化替代的步伐。根據資料,截止2019年8月30日,共批準了233個產品申請項目進入特別審批程序。其中2019年批準了28項,血管介入類獨占5項(去除診斷類)。
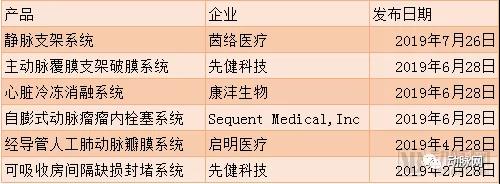 (截止目前,2019年血管介入領域創新醫療器械中進入特別審批程序的產品)
審批產品中,從產品類型上看,以植介入器械等高值耗材為主的產品占比最高,尤其是血管介入類產品中的血管支架。目前已有4款血管支架通過創新醫療器械特別審批程序上市,分別為上海微創醫療的分支型主動脈覆膜支架及輸送系統,北京華脈泰科的腹主動脈覆膜支架系統,樂普醫療的生物可吸收冠狀動脈雷帕霉素洗脫支架系統,微創心脈的腹主動脈覆膜支架及輸送系統。
2017年,百心安、阿邁特、信立泰和脈全的生物可吸收冠狀動脈雷帕霉素洗脫支架系統也被納入了特別審批程序。
除此之外,國內眾多創新產品進入臨床試驗階段,如卵圓孔未閉封堵器等。諸多利好因素促使資本對醫療產業增加信心,不減對于醫療產業的投資。
血管介入類器械與耗材市場情況
高值醫用耗材是指技術要求高、監管嚴格、限于某些專科使用且價格較高的消耗性醫療器械,包括心血管類、骨科類、眼科類、口腔類。其中,血管介入類耗材包含心臟支架、導絲、導管等。
國內發展較好的該領域企業包括樂普醫療、微創醫療等,而優秀的創新企業也在不斷獲得認可,如博邁醫療。
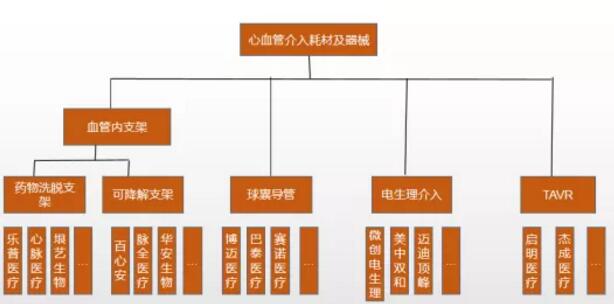 (部分血管介入類產品及相關企業)
高值耗材在全球醫療市場中占據較大比例,根據統計,2017年心血管類高值耗材位列全球第二大器械細分領域。相比之下,國內醫療器械市場高值耗材占比較低,心血管類占比僅為6%,前景較大。
目前,針對心血管疾病,臨床上主要采用藥物治療、外科手術與介入治療三種手段。介入治療憑借其創傷小、恢復快、住院時間短等優點,已成為適應癥的首選。這也促進了血管類介入耗材的快速發展。
據測算,我國醫療器械市場規模從2006年的434億元增至2018年的5304億元,年均復合增長率約為25.55%。其中,高值醫用耗材的市場規模約為1046億元,同比增長20.37%,是醫療器械細分領域中增長率最高的一個。
同時,我國心血管病現患病人數2.9億,隨著社會老齡化程度的加深,未來我國心血管病患病率和死亡率都處于上升階段。另外,新農合的實際報銷比例不斷提高,基層醫療水平的不斷提升,基層PCI手術的需求將得到釋放。這些因素都將讓中國心血管高值耗材市場保持快速增長,市場增速預計仍將保持20%左右的高增長率。
 (動脈網根據相關數據整理)
從市場情況來看,醫用高值耗材市場中,以強生、美敦力等為代表的國外廠商在中高端產品領域競爭激烈,國內廠商在國家推動國產化替代的進程中,創新力不斷提升,創新產品不斷涌現,市場占比逐步上升。
國內布局血管介入器械的大公司包括樂普醫療、微創醫療、先健科技、垠藝生物、美中雙和、微創電生理等。這些公司的研發實力強勁,其研發的血管支架是我國高端醫療器械中少有的基本實現了國產替代的產品。
在這些公司中,先健科技、垠藝生物、美中雙和以及微創電生理專注于心血管介入領域,先健科技的封堵器、微創電生理的三維標測系統和射頻消融導管等都是全國乃至世界領先的。除此之外,創新性公司也有突破性進展。例如,心臟瓣膜領域的啟明醫療、人工心臟領域的蘇州同心、載藥微球領域的蘇州迦利生(2015年被恒瑞醫藥收購)等。
創新產品方面,先健科技、微創醫療都有多款產品被納入創新醫療器械特別審批名單,其中,先健科技已有一個封堵器產品和一個起搏器產品獲批,微創醫療包括旗下微創電生理共有三個產品獲批。國內還有唯柯醫療、唯強醫療等一批企業進行創新性研究,未來兩年內,將有一批創新性產品上市。
但是目前,血管介入耗材僅冠脈藥物支架實現進口替代,勁動脈支架、遠端保護器、心臟起搏器、外周血管支架、支架材料等介入產品及材料進口比例高達80%-100%。
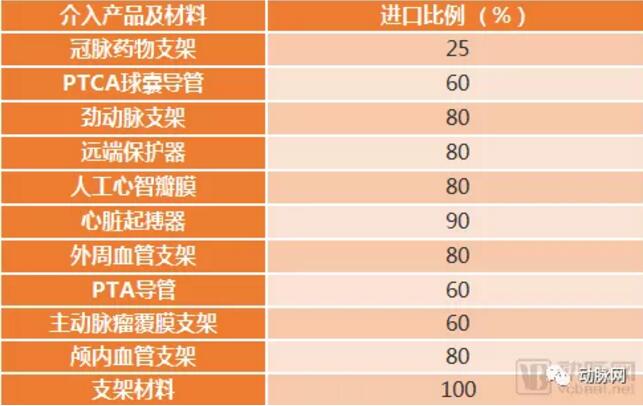 (動脈網根據相關數據整理)
人口老齡化程度的不斷加深,國民生活水平不斷提高以及醫保覆蓋范圍及深度的提升,帶來介入類手術需求的增加,使得我國對高值醫用耗材需求持續增加。政策端鼓勵醫療器械創新和技術升級,為國產創新醫療器械開辟了綠色通道。需求端和政策端共同推動國內高值耗材市場快速發展。
進口替代是指用本國產品替代進口產品。根據前瞻產業研究院數據,2017年我國醫療器械進出口總額為420.6億美元。從醫療器械進口結構來看,中高端醫療器械約占全部進口醫療器械的44.3%,其中進口金額排名前三的醫療器械分別是光學射線儀器、高端介入類材料以及醫用X射線診斷設備。
高端介入耗材中,心臟支架自2010年起,國產支架已占有國內80%的市場,圓滿完成進口替代任務。除此之外,其他細分市場仍然以進口產品為主。國內企業如何提高國產產品市場占有率成了重要問題,從業者對此十分關注。
現根據大家廣泛關注的熱點,動脈網以血管介入耗材為例,采訪了華山醫院心內科潘俊杰教授、德諾醫療CEO趙亦偉先生、博邁醫療CEO李斌先生以及經銷商,探討分析進口替代大背景下,國產高值耗材如何提高市場話語權。
潘俊杰教授自2000年來一直從事臨床一線工作,具有豐富的心血管疾病診療經驗,對心內科危重癥疾病的搶救有獨到的經驗。尤其是對冠心病復雜病變的支架植入有較深的理解和造詣,每年獨立完成急診及平診手術300多例。
德諾醫療是一家專業的創新生命科技產業投資、孵化及運營企業,在中國和美國都設有研發中心。旗下擁有啟明醫療、堃博生物、唯強醫療、諾茂醫療、德晉醫療、德柯醫療等創新性企業。
廣東博邁醫療器械有限公司是一家專業從事血管介入高值耗材的設計、生產、銷售和服務的醫療器械生產企業,產品行銷包括歐美日在內的40多個國家和地區。
國內企業遇到的問題
政策上阻擋國產優秀產品與進口產品公平競爭
曾經國產產品技不如人時,政府招標時會刻意將進口產品與國產產品分開競標,這在以前可以保護國產產業擁有一定的市場機會,但是現在,這是阻礙國產優秀血管介入耗材與國際品牌平等競爭的一座大山。
事實上,中國醫療器械產業進步十分迅速,很多產品如今已比國外普通企業的產品質量更好。但是由于競標時國產產品不能與進口品牌競爭,國內政策保護了進口產品,導致國內企業在競爭中處于劣勢地位。
以博邁醫療為例,其產品已在中國、美國、歐盟、日本等地注冊,并在40多個國家和地區規模銷售,在多個發達國家與國際一線品牌同臺競爭。但是,能在國際市場競爭中擊敗眾多國際一線產品的博邁醫療球囊導管,回到中國后,只能被限制在國產產品中殺價競爭,而市場分額也被限制在一個小范圍中。
如果在國內產品的技術和質量取得明顯進步后,政策能夠與時俱進,及時調整,那對于實現血管介入醫療器械的進口替代的規模和速度一定有巨大幫助。
國產創新產品不僅質量過關,而且更貼近中國臨床,可以更快速的響應中國臨床的需求。但是市場上還是進口產品為主流。這就需要政策順應時事,盡快改變。
優秀產品較少,質量普遍弱于進口產品
這些年,國產血管介入耗材的質量進步很大,例如心臟支架,有些支架甚至與進口產品不相上下,從隨訪情況來看,效果也相差無幾。但是從客觀上講,還有很多國產產品與進口產品相比,在精細度方面還存在一定差距。
例如導絲、導管等配件,如果是工藝簡單的產品,國內外品牌基本沒有區別,但是針對復雜病變的產品,國產產品在質量上比不上進口產品。
血管介入耗材中的導絲,直徑非常小,其工藝要求十分高。我國在精工制造方面積累的經驗還不夠,還需要繼續打磨或者完成技術突破。導絲產品中,日本的產品做到了全球頂尖。為什么日本的產品十分受歡迎呢?
華山醫院潘俊杰教授表示:“因為日本的醫生不斷反饋使用效果,企業工程師團隊不斷改進產品,兩者之間形成了閉環,促進了導絲的升級換代。同時,日本的精工工藝發展早,實力強,其孜孜以求的工匠精神十分值得我們學習。”
除了精工制造的經驗欠缺外,國產導絲質量稍差,可能還與投入研發生產的資金有關。導絲的市場價格低,技術含量高,投入產出比不高。因此,企業在生產導絲時可能考慮前期投入太大,產出不夠明顯,不愿意研發高質量產品。
一位不愿意透露姓名的經銷商表示:“無論是進口產品還是國產產品,醫生選擇產品的唯一標準就是質量。國內企業在研發產品時會與醫生合作,但是醫生不是研發者,并不能準確表達出自己的想法。舉個例子,醫生會說某個產品使用起來有點硬,但是具體數據是多少,工程師無法體會。”
日本的企業生產產品時追求精益求精,醫生會不斷的反饋使用效果,工程師則不斷的優化改進產品,扎扎實實,共同將產品做好。因此,日本的血管介入耗材在全球市場上十分受歡迎。
模仿技術多,創新技術少
血管介入耗材的國產化還有很大的潛力,比如高鐵、通信等其他行業,都已做到世界領先,而醫療行業也肯定有潛力做到世界領先。
血管介入耗材具有非常明顯的技術壁壘,在這個領域,技術為王。醫療行業總是在不斷完善新技術,企業總是在迭代更新產品。如果國內企業永遠跟在別人后面仿制技術,那么這些企業很難發展壯大。
雖然,前期仿制國外技術可以很快獲利,但是長遠來看,模仿國外技術沒有企業自己的核心競爭力。而且醫療行業不同于一般行業,仿制產品上市速度慢,還會遇到專利訴訟等問題。
德諾醫療CEO趙亦偉先生介紹:“醫療行業專利保護更嚴格,產品上市需要經過研發、臨床試驗、申請注冊證等多個步驟,需要很長時間的審查。當仿制產品上市后,原創企業已經占領大部分市場,甚至已經發布第二代產品。患者對品牌也已經形成信任,仿制產品難以撼動。”
對于使用原創產品的臨床醫生而言,培訓醫生的往往都是技術先行者。因此,原創企業培訓過醫生后,這些醫生已經對疾病的認知、解決方案、手術操作等形成習慣。當仿制技術出現后,醫生沒有足夠的積極性去學習仿制技術。
綜合因素累計起來,形成原創技術碾壓仿制產品的局面。因此,醫療行業的國產化水平還需要繼續提升,還需要鉆研創新性技術。
進入市場晚,難以撼動進口品牌
除了質量之外,手感也是一個很重要的因素。醫療產品多是用手操作,這就需要生產廠家考慮醫生的使用手感與習慣。做手術不像開車,寶馬或奔馳,一般人察覺不出區別,但是醫生常用介入產品,對產品的手感很敏感。例如導管,醫生操作遠端,頭端在患者血管內會做出相應反應。如果做不到“指哪打哪”,醫生不會喜歡這個產品。
有些產品并不是質量不合格,而是很多醫生已經對某種品牌的產品形成習慣,如果突然換一種產品,醫生在手術時會受一定影響。也許只是差之毫厘,但是可能造成手術失敗。因此,一般情況下醫生不會隨意更換品牌。
博邁醫療CEO李斌認為,血管介入耗材國產化最大的難點就是觀念。他認為從臨床醫生到監管部門,都有一個根深蒂固的觀念:進口的產品一定好,國產的產品一定差。“其實回顧改革開放40年,中國大多數工業行業都是如此。例如手機行業,華為手機沒有經過多代的蛻變驚艷而出前,估計很少有人相信中國的手機會比三星、蘋果更受歡迎。而醫療健康產品由于事關人身安全,所以觀念的改變更是謹慎而緩慢。”
其實,這也是多年來進口產品對用戶進行品牌宣傳的效果。這種觀念是從以前國產產品質量普遍較差或市場上沒有國產產品的時候培養的。進口產品進入市場較早,首先對用戶進行培育,使其相信進口產品的質量總是優于其他,這使得近年來逐步提升品質的國產產品難以撼動市場。
臨床醫生擔心國產產品的安全性與有效性
事實上,使用進口產品最多的醫院是國內著名的大醫院。國內大醫院的醫生遇到的疾病更加棘手,病變更加復雜,如果使用國產產品,可能出現再狹窄等問題,或者沒有達到醫生預期的治療效果。在這些大醫院就診的患者,基本上也已經拋開了價格的問題,患者家屬更在意治療效果。因此,這些大醫院使用進口產品是必然選擇。
例如導管,醫生做介入手術時,需要將支架等產品輸送到病變位置,但是由于導管壁太厚或導管的內腔太小,支架等產品難以通過。
如果出現上述問題,患者就會有生命危險,手術也難以完成,醫生會陷入兩難的局面。當手術失敗,醫生將會面臨家屬的責問,需要處理各種各樣的糾紛。醫生也因此難以專心做好本職工作,這對于醫生的影響很大。因此,醫生以病人的利益為最高目標,選擇某個產品都是為了更好的完成手術(治療)。無論是從患者還是醫生的角度,醫生都希望使用質量更好的產品。
國產品牌為什么難以推廣?血管介入耗材是拯救生命的產品,是世界上風險等級最高、監管最嚴格的產品之一。因此,血管介入耗材不會出現高、中、低檔等不同的市場。其他產品可以選擇低檔產品,而血管介入耗材則必須選擇療效好、質量高的產品。醫生不會因為某個產品價格低就使用,患者家屬也希望使用效果與質量最好的產品。
市場上如果出現了一個更先進的產品,落后的產品很難說服市場,只會出現贏者通吃的局面。從本質上講,市場不會允許醫療產品只顧及價格而降低安全性與有效性。
國產產品的出路在哪
政策上扶持醫療行業及國產產品
國產心臟支架比進口支架價格低,進口支架約15000元一個,而國產支架大約7000-8000元一個。除此之外,其他血管介入耗材在價格上并不低于進口產品,在價格上并不存在優勢。如果政府能夠對醫保支付政策進行改革優化,做到既能降費,又能支持國產優秀器械,對于國產品牌而言會是重大利好。
在產業政策中,政府如果加大對醫療行業的支持,國內企業有可能增加對于高端醫療產品的研發,提高國產產品的品質與質量,使得國產品牌有機會在國內市場贏得一定的話語權。
在美國,醫藥行業占美國GDP的20%,而在中國,醫藥行業僅占GDP的5%。醫藥行業作為朝陽產業,需要國家更多的關注。如果醫藥行業得到政策扶持,中國的技術型企業、創新性企業能夠發展,醫療產品的國產化將指日可待。
幸運的是,近半年時間,國家相繼出臺高值耗材治理方面有關政策。例如《關于治理高值醫用耗材的改革方案》《醫療器械唯一標識系統試點工作方案》《治理高值醫用耗材改革方案》等政策陸續發布;江蘇率先開展省級聯盟采購高值耗材;11月6日,國家發展改革委公布了《產業結構調整指導目錄(2019年本)》。
江蘇集中采購規則中,此次有資格參與帶量采購的品種,均是近5年來江蘇省醫用耗材集中采購省級評審入圍產品,經過多年臨床驗證,安全可以得到保障。對于連續出現質量問題的入圍產品,聯盟也有退出機制。
醫療器械不同于藥品,難以進行一致性評價,但是經過多年臨床驗證的產品才有資格參與帶量采購的規定,對于創新性企業、初創企業,是一重大打擊。
11月6日公布的《指導目錄》指出,醫藥領域鼓勵高端設備的研發制造,其中包括新型支架、假體等高端植入介入設備與材料。《產業目錄》由鼓勵類、限制類、淘汰類三個類別組成,具體到醫藥領域,涉及鼓勵類目8項、限制類目6項、淘汰類目13項。
鼓勵類主要是對經濟社會發展有重要促進作用,有利于滿足人民美好生活需要和推動高質量發展的技術、裝備、產品、行業;
限制類主要是工藝技術落后,不符合行業準入條件和有關規定,禁止新建擴建和需要督促改造的生產能力、工藝技術、裝備及產品;
淘汰類主要是不符合有關法律法規規定,不具備安全生產條件,嚴重浪費資源、污染環境,需要淘汰的落后工藝、技術、裝備及產品。
《產業目錄》明確自2020年1月1日起施行。這對于創新性企業是一重大利好。有專家表示:“面對行業陣痛期,唯有創新是突圍希望。
技術上不斷創新
醫療技術在不斷創新,國內企業如果能抓住技術變化中的趨勢,在技術上下足功夫,不斷鉆研突破,這個行業就有機會出現跳躍式的發展,國產品牌才有可能進入全球第一梯隊。
目前,國產產品質量提升,技術進步,已具備替代進口產品的能力。但是國內企業對于創新性技術的鉆研還需要加大投入,提升自己的核心競爭力,未來才能跟得上國際步伐。
例如,德諾醫療十年前就開始布局新興領域——結構性心臟病。該領域,國內外都處于起步階段。處于同一起跑線,德諾醫療憑借優秀的團隊,不斷研發出新產品。而正是因為其創新性技術,德諾醫療的產品才能夠占領市場,獲得專家、醫生、患者認可。
導絲等精細產品,隨著國內工藝技術的提升,國產產品的質量也在不斷升級。目前,國家政策支持國產產品的使用,醫生也會在可能的情況下多使用國產品牌,國產產品的使用量也因此會不斷增加。
注重同業宣傳
一位經銷商表示:“宣傳推廣血管介入耗材的作用并不大。”國內公司推廣產品時總是宣稱不亞于某款產品,自然表明了也不會超過這款產品,技術上沒有突破,價格上也沒有很大優勢,醫生很難選擇推廣的那款產品。只有比其他產品質量更好,技術更過硬,醫生才會選擇使用。
曾經有一家國際性器械廠商生產了一款導絲,當時推廣的口號是宣稱不亞于日本某品牌。但是到目前為止,市場上使用該產品的醫生并不多。
還有一部分國內企業在宣傳推廣時,會選擇突出某種先進技術,但是真正臨床使用后,很明顯就可以評價一個產品的好壞。醫療產品不同于其他產品,其用于患者后會出現并發癥及其他問題,在臨床或隨訪時,會有很直接的反饋,可以明顯看出產品的效果如何。
其實很多進口產品并沒有做推廣,而是通過口碑與業內宣傳來帶動銷量。國產產品也有類似的案例,例如微創的支架,由于質量好,醫生認可,從而贏得市場。因此,醫生更看重同業宣傳,更看重同行對某款產品的意見。
要想促進血管介入耗材國產化,需要國內企業把產品質量提高,并與醫生合作,不斷優化使用手感。當醫生認可國產產品時,國產產品自然會有更高的銷量,國產化也是自然而然的事情。
臨床上試用國產創新產品
對于一些簡單的病變,臨床醫生可以選擇國產產品,但是對于復雜的病變,操作比較困難,可以選擇精細程度更高的進口產品或國內優秀創新性產品。
以華山醫院為例,心臟支架由于國產產品的質量與進口產品不相上下,因此使用國產產品比例更高。導絲等精細產品,對于簡單的病變會選擇試用國產產品,如果試用效果好,醫生會繼續使用該產品;如果使用時存在瑕疵,醫生會給廠家一些建議,幫助其優化改進。這對于國產產品實現國產化有一定幫助。
國內有一批創新性企業,也有一批優秀產品。其性能經過國外體系、國際市場的驗證,不但不輸于進口產品,甚至比部分進口產品更好。如微創醫療、樂普醫療、啟明醫療等等。
因此,國內臨床上應當給予國內企業機會,讓更多優秀產品替代進口產品,用于復雜的病變,讓普通產品用于簡單的病變。如此,國產產品市場占有率越來越高,質量越來越高,臨床效果越來越好,形成良好的循環。
血管介入耗材領域國內企業的布局
啟明醫療布局TAVR技術
經導管主動脈瓣膜置換術(TAVR)是指將組裝好的主動脈瓣經導管置入到主動脈根部,替代原有瓣膜發揮功能。與外科手術相比,TAVR 具有創傷小、恢復快等優勢,未來隨著瓣膜技術的持續改進與醫生治療經驗的積累,TAVR 有望成為主動脈瓣膜置換的主流術式。
從全球來看,愛德華與美敦力兩家國際巨頭各自瓜分了TAVR全球65%與30%的市場。不過,啟明醫療自主研發的 VenusA-Valve 經導管人工主動脈瓣膜置換系統在2017年獲準上市。截止目前,啟明醫療通過經股動脈路徑植入瓣膜2600例,進口替代的形勢讓人樂觀。
國內布局TAVR技術的除了啟明醫療之外,還有杰成醫療、微創醫療等。我國雖然起步較晚,但在國家政策、創業者和資本的助力之下,正在大跨步前進。
隨著TAVR技術逐漸在頂級醫院普及,心臟瓣膜的潛在需求也正逐漸浮現。華泰證券數據顯示,截止2018年底,有80余家醫院具有TAVR手術經驗。隨著該技術進入更多的醫院,國內市場預計將在2029年超過百億。除了經導管主動脈瓣膜產品,啟明醫療還布局了經導管肺動脈瓣膜等產品。
德諾醫療布局結構性心臟病與外周血管等
德諾醫療十年前就開始布局新興領域——結構性心臟病。該領域,國內外都處于起步階段。處于同一起跑線,德諾醫療憑借優秀的團隊,不斷研發出新產品。而正是因為其創新性技術,德諾醫療的產品才能夠占領市場,獲得患者認可。
德諾旗下諾誠醫療的Liwen RF射頻消融系統、啟明醫療的經導管主動脈瓣膜產品Venus A-Valve、唯強醫療的模塊內嵌主動脈弓覆膜支架、諾生醫療的NoYA可調式心房間分流系統、諾茂醫療的SeaLA左心耳封堵器等等,都具有不同的優勢。
例如,唯強醫療的模塊內嵌主動脈弓覆膜支架針對主動脈弓部疾病。弓部疾病發病率相對較高,且弓解剖結構復雜。主動脈腔內介入治療的難點是主動脈弓部疾病被隔絕的同時,保證弓上分支血管的通暢。患者腦部供血一旦缺血時間較長,將造成致命的傷害。這款支架包含多個模塊支架,植入過程不影響主體血管和分支血管的血供,手術危險性大大降低。
博邁醫療布局先進制造工藝
博邁醫療致力于通過將國際領先的產品技術和制造工藝技術與創新型的開放性商業模式相結合,實現國產品牌在全球高端醫療器械耗材市場的優勢競爭地位。
其研發的冠脈球囊擴張導管擁有目前全球最小穿越狹窄病變的外徑,可以穿越CTO復雜病變。而其研發的三導絲刻痕球囊擴張導管,具備卓越的擴張病變和穿越病變的能力。
博邁醫療自主研發的Artimes及Apollo球囊擴張導管,從產品的設計,到產品的質量與性能,都處于國際一流的水平。這兩個產品主要應用于為改善冠狀動脈的局部狹窄病變處的心肌血流而實施的經皮冠狀動脈腔內血管成形術。
截止目前,博邁醫療的冠脈球囊擴張導管產品已經在包括中國、美國、歐盟、日本等超過40個國家和地區規模銷售,在多個發達國家與國際一線品牌同臺競爭,甚至在部分國家,博邁醫療產品的市場占有率已經超過部分國際一線產品。除上述產品外,博邁醫療還在心血管介入、外周血管介入、血管通路等領域研發出了多款產品。
國內除了創新企業的創新產品,還有實力雄厚的大公司如樂普醫療、微創醫療、吉威醫療、心脈醫療、先健科技、佰仁醫療等諸多企業與國際品牌進行競爭。從長遠來看,血管介入耗材國產化也是必然的趨勢。
結語
通過與臨床專家、企業、經銷商的交流,動脈網認為血管介入耗材國產化有以下幾個舉措可供參考:
1、企業選擇從基層醫院開始推廣,并邀請醫生進行業內宣傳;
2、企業可邀請專家試用優秀產品,并根據反饋進行優化,替代進口產品;
3、臨床醫生多使用優秀國產產品,給國產企業一定機會;
4、國家扶持醫療產業,促進醫療行業的發展;
5、醫療器械的集中采購政策要創新,在保證質量的情況下選擇低價產品,可考慮請專家委員會試用競標產品,通過試用后進行議價,采購保護期可考慮延長至兩年。
6、國家可鼓勵試用創新性產品,保護初創企業的發展。
目前,中國制造的能力在不斷增強,國產產品的質量不斷提升。我國的產品也已出口至非洲、東南亞等國家。政策導向下,國產產品的使用比例越來越高,目前的數據已經有所體現。血管介入耗材的國產化在多個措施不斷推進下,效果正在逐步顯現。
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|