
|
|
|||||
|
||||||
CE認證、FDA認證怎么拿?市場監管總局版指南上線!摘要:
醫藥網4月7日訊 目前國內企業向歐盟、美國等國出口口罩需要通過歐盟的CE認證、美國FDA注冊程序。采訪中,記者了解到,目前很多企業并不了解這個信息,不知道哪些機構具備相應資質,很多企業盲目委托中介機構申請國外認證,甚至出現排隊辦理出口認證的情況,有的企業還遭受損失。
4月5日,國家市場監督管理總局認證監管司司長劉衛軍在“國務院聯防聯控機制新聞發布會”上介紹,經過初步梳理,已經編制出一份口罩等防疫產品出口到歐盟和美國的認證信息指南,在市場監管總局、國家認監委的網站,以及公眾號上都可以看到。
劉衛軍介紹,這份認證信息指南包括歐盟CE標志、美國FDA注冊等相關要求。這份指南還為企業提供了快速、直接了解這些要求以及解決問題的途徑。
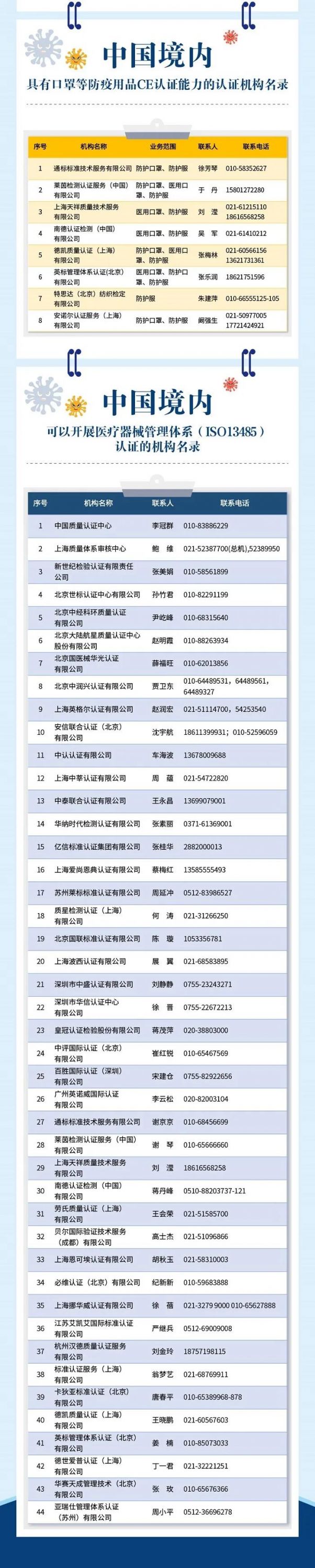
另外,有些進入歐盟的產品,需要經過歐盟授權的公告機構的認證,在中國都有哪些機構能夠做這項業務?在指南里也列出了這些機構的名錄。在醫療器械領域,國際上還有ISO13485醫療器械管理體系的標準,企業需要獲得這個體系認證。哪些機構能做這項工作?指南里也有相應的信息。
這份指南今后還會不斷更新,為企業提供便利,幫助企業解決實際困難。
“假證”舉報撥打12315
采訪中,記者了解到,現在網上“花錢”就能辦到CE證書的“假宣傳”層出不窮。如果企業遇到這種辦證的情況,辦了假證應該怎么辦?
劉衛軍表示:“疫情發生以來,市場監管總局特別注重對防疫產品認證的違法違規行為進行查處,現正在查處冒用認證標志、虛假宣傳認證信息的案件。”
他表示,特別是針對現在出口的一些不規范認證行為,市場監管總局專門部署要開展專項整治行動,《關于開展口罩、防護服等防疫用品領域認證活動的專項整治行動的通知》已經正式下發,整治重點主要有偽造冒用買賣認證證書、未經批準擅自從事認證活動、認證活動不規范以及認證價格違法的行為。
以去年為例,市場監管總局查處了87家違規認證機構,占認證機構總數的15%,其中5家問題嚴重,直接撤銷了資質。另外,2家國外的認證機構在中國沒有經過批準,就非法開展認證活動,已經在網上進行了警示公告。對電商平臺銷售的認證產品,市場監管局也加強了核查,去年電商就下架了17000多件相關產品。
如果遇到類似問題,市場監管局提示,可以撥打12315投訴舉報熱線,或者12315網絡平臺,都可以進行投訴舉報。
機構選擇至關重要
劉衛軍提醒道,第一,一定要找合法的認證機構。中國現在經過批準的有600多家認證機構,從事產品、服務、管理體系等認證,這是指所有的認證活動,不僅僅針對出口。這些信息在國家認監委的網站上都可以查詢到,企業如果要做認證,一定要找具有相應合法資質的機構,千萬別被不良機構給忽悠了。
第二,一定要了解出口目的國的市場準入要求。指南里也作了一些這方面的說明,比如出口到歐盟的醫用口罩分兩類,一類是無菌的,一類是非無菌的。對非無菌醫用口罩,歐盟規定只要企業按照相關要求作出符合性自我聲明,就可以加貼CE標志。而對無菌醫用口罩,就必須找歐盟授權的機構才能獲得真正的CE認證,產品才能進入到歐盟市場。如果是輸往美國,企業可以按照美國的管理規定,通過FDA的網站申請并提交相關材料。
第三,出口企業一定要按照我國和目的國的規定開展生產經營活動,加強產品質量管理。商務部、海關總署、藥監局前幾天剛發布公告,明確要求相關醫療物資出口必須獲得我國醫療器械產品注冊證書,同時要滿足進口國(地區)的質量標準要求。
劉衛軍還指出:“如果真是出口中出現了質量方面包括認證評價的問題,一定要積極回應,特別是對那些不實信息和炒作,要積極進行回應,消除誤解,這樣既保護企業自身利益,也維護中國產品的信譽和形象。”
嚴管五類產品出口
海關統計數據顯示,3月下旬以來,出口疫情防控物資增幅比較大,從3月1日到4月4日,全國共驗放出口主要疫情防控物資價值102億元,主要包括口罩約38.6億只,價值77.2億元;防護服3752萬件,價值9.1億元;紅外測溫儀241萬件,價值3.3億元;呼吸機1.6萬臺,價值3.1億元;新型冠狀病毒檢測試劑284萬盒,護目鏡841萬副。
從貿易方式情況看,主要還是一般貿易,占了約83%,價值85.2億元。
商務部外貿司一級巡視員江帆介紹,為深化國際疫情防控合作,加強醫療物資出口質量的監管,3月31日,商務部會同海關總署、藥監局發布了《關于有序開展醫療物資出口的公告》,要求出口的檢測試劑、醫用口罩、醫用防護服、呼吸機、紅外體溫計等五類產品,必須取得我國醫療器械產品注冊證書,符合進口國(地區)的質量標準要求,海關憑藥監部門批準的醫療器械產品注冊證書驗放。
另外,為做好疫情防控用醫療器械的質量監管,國家藥監局與其他部門積極配合,通力合作。會上,國家藥品監督管理局器械監管司副司長張琪也指出,一是強化監督檢查。加強對生產企業原材料采購、生產過程控制、產品出廠放行等重點環節的監督檢查,督促企業嚴格依照法規要求和標準組織生產。對發現的問題,責令企業整改到位,堅決防止不合格產品流入市場,從源頭上保障醫療器械質量安全。
二是強化質量檢驗。截至3月底,共開展針對疫情防控醫療器械的應急注冊檢驗、應急評價檢驗以及監督抽檢等各種形式的檢驗共計8069批次,總體質量狀況符合要求。
三是強化督導檢查。國家藥監局、市場監管總局選派多名精干執法人員赴北京、天津、浙江、湖北、廣東等14個重點省份,對疫情防控醫療器械質量監管工作進行督導檢查,督促各項工作抓實抓細抓落地。
四是嚴厲打擊違法違規行為。國家藥監局等八部門聯合組織開展嚴厲打擊制售假劣醫療器械違法行為,切實保障防控醫療器械質量安全。有關案例查處情況已在國家藥監局網站上公布。
五是及時公開注冊信息。對獲得批準的產品相關注冊信息,在國家藥監局網站公布,并根據審批情況及時更新,為采購方選擇提供參考,也為相關部門開展出口監管工作提供便利。
  |
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|