
|
|
|||||
|
||||||
突襲檢查!知名醫(yī)械公司被查,多家遭停產(chǎn)!摘要:
醫(yī)藥網(wǎng)10月23日訊
突襲檢查!4家械企遭停產(chǎn)整改
國家級飛檢,是國家級檢查組千里奔襲的突擊檢查,目的就是為了指出企業(yè)問題,督促企業(yè)生產(chǎn)質(zhì)量管理體系進行持續(xù)改進。
10月20日,國家藥監(jiān)局發(fā)布《關(guān)于青海登士達醫(yī)療器械有限公司等4家企業(yè)飛行檢查情況的通告(2020年 第71號)》。
 青海登士達醫(yī)療器械有限公司、浙江金華星期一生物技術(shù)有限公司、深圳市海博科技有限公司、北京福愛樂科技發(fā)展有限公司,4家企業(yè)因質(zhì)量管理體系存在嚴重缺陷,不符合醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范相關(guān)規(guī)定,國家藥監(jiān)局已經(jīng)責令上述企業(yè)立即停產(chǎn)整改。
對涉及違反《醫(yī)療器械監(jiān)督管理條例》及相關(guān)法律法規(guī)的,依法嚴肅處理;屬地省級藥品監(jiān)督管理局責令企業(yè)評估產(chǎn)品安全風險,對有可能導致安全隱患的,按照《醫(yī)療器械召回管理辦法》的規(guī)定召回相關(guān)產(chǎn)品。
從《通告》內(nèi)容來看,上述4家醫(yī)械企業(yè)存在機構(gòu)與人員方面、質(zhì)量控制方面、生產(chǎn)管理方面、設(shè)備方面等相關(guān)問題。
 國家局通報!知名醫(yī)械公司被查
同樣在本月13日,國家藥監(jiān)局核查中心發(fā)布《醫(yī)療器械飛行檢查情況通告(2020年第2號)》。
國家藥監(jiān)局核查中心于2020年8月-9月組織開展了醫(yī)療器械生產(chǎn)企業(yè)飛行檢查工作,發(fā)現(xiàn)13家醫(yī)療器械企業(yè)存在不符合《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》及相關(guān)附錄的問題。13家械企共被檢查出112家缺陷。
13家被飛檢企業(yè)情況匯總
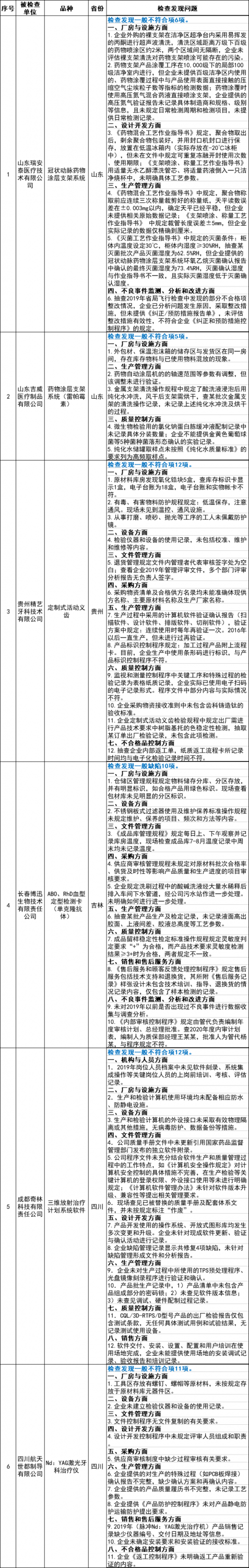 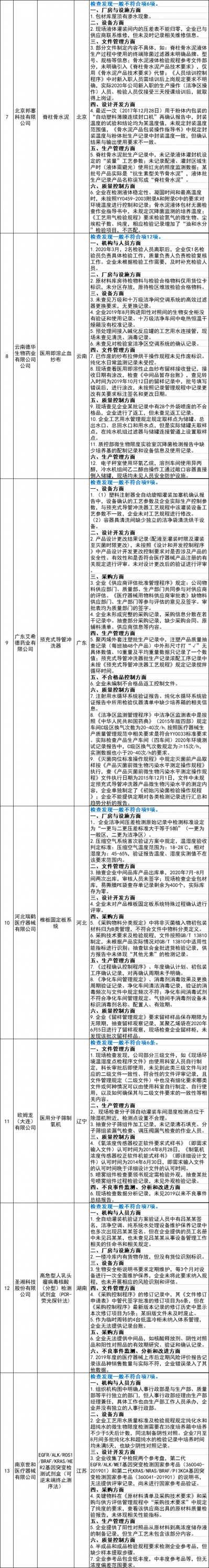 針對檢查中發(fā)現(xiàn)的問題,上述通告要求相關(guān)省(自治區(qū)、直轄市)藥品監(jiān)督管理局應(yīng)責成企業(yè)限期整改,要求企業(yè)評估產(chǎn)品安全風險,對有可能導致安全隱患的,應(yīng)按照《醫(yī)療器械召回管理辦法》的規(guī)定召回相關(guān)產(chǎn)品。
企業(yè)完成整改后,相關(guān)省藥品監(jiān)督管理局應(yīng)及時組織跟蹤復查,并將跟蹤復查情況及時報送國家藥品監(jiān)督管理局食品藥品審核查驗中心。
本次飛檢涉及山東瑞安泰醫(yī)療技術(shù)有限公司、山東吉威醫(yī)療制品有限公司、貴州精藝牙科技術(shù)有限公司、長春博迅生物技術(shù)有限責任公司、成都奇林科技有限責任公司、四川航天世都制導有限公司、北京邦塞科技有限公司、云南德華生物藥業(yè)有限公司公司、廣東艾希德藥業(yè)有限公司、河北瑞鶴醫(yī)療器械有限公司、歐姆龍(大連)有限公司、圣湘生物科技股份有限公司、南京世和醫(yī)療器械有限公司。
其中歐姆龍國內(nèi)子公司歐姆龍(大連)有限公司,其醫(yī)用分子篩制氧機被檢查發(fā)現(xiàn)一般不符合項6條。
這家外資巨頭國內(nèi)子公司,飛檢被查出問題,對于其影響不可謂不小。這也給企業(yè)敲響警鐘,加大各個環(huán)節(jié)的自查,至關(guān)重要。
國家檢查員再增58人!突襲檢查頻率增加
不難發(fā)現(xiàn),開年以來各省檢查組紛紛加大檢查頻次,加大對省內(nèi)生成企業(yè)、經(jīng)營企業(yè)以及終端醫(yī)院的檢查。
而這也正是由于去年,國家藥監(jiān)局發(fā)布《關(guān)于建立職業(yè)化專業(yè)化藥品藥品檢查員隊伍的意見》。
文件強調(diào),職業(yè)化專業(yè)化醫(yī)療器械檢查員是指經(jīng)藥品監(jiān)管部門認定,依法對管理相對人從事藥品研制、生產(chǎn)等場所、活動進行合規(guī)確認和風險研判的人員。
具體來看,國務(wù)院監(jiān)管部門主要醫(yī)療器械研發(fā)過程現(xiàn)場檢查,會從醫(yī)療器械臨床試驗質(zhì)量管理規(guī)范執(zhí)行情況合規(guī)性檢查。承擔醫(yī)療器械境外現(xiàn)場檢查以及生產(chǎn)環(huán)節(jié)重大有因檢查。
而省級藥品監(jiān)管部門主要醫(yī)療器械生產(chǎn)過程的現(xiàn)場檢查,以及有關(guān)生產(chǎn)質(zhì)量管理規(guī)范執(zhí)行情況合規(guī)性檢查。
省級部門還將對醫(yī)療器械批發(fā)企業(yè)、零售連鎖總部、互聯(lián)網(wǎng)銷售第三方平臺也將進行相關(guān)現(xiàn)場檢查。可以看出國家針對醫(yī)療器械領(lǐng)域的各個環(huán)節(jié),各個渠道都做了部署。
就在不久前,國家藥監(jiān)局再次公布了新一批《關(guān)于聘任第五批國家醫(yī)療器械檢查員名單》。58人被聘為第五批國家醫(yī)療器械檢查員,分布在全國多個省份。未來還將有更多國家檢察員趕赴全國各地,這種不打招呼直奔現(xiàn)場的檢查頻次將會越來越高!
 |
|
Copyright ?2015 廣東穗康醫(yī)藥有限公司
粵ICP備15022662號(粵)
-技術(shù)支持:信息管理部|聯(lián)系我們
|