
|
|
|||||
|
||||||
藥企排行榜公布:恒瑞、齊魯、百濟神州…摘要:
醫藥網3月2日訊 2021年伊始,中國藥品監督管理局藥品審評中心便發布了《生物類似藥相似性評價和適應癥外推技術指導原則》,為進一步規范和指導生物類似藥研發和評價,為工業界、研究者及監管機構提供技術參考。這使得生物藥研發越來越成為藥物研發中的重點項目,那么今天我們就根據藥智網《2020中國生物藥研發實力排行榜》,跟隨國內生物藥研發“大佬”一起來看看他們的管線分布。
 上海復星醫藥
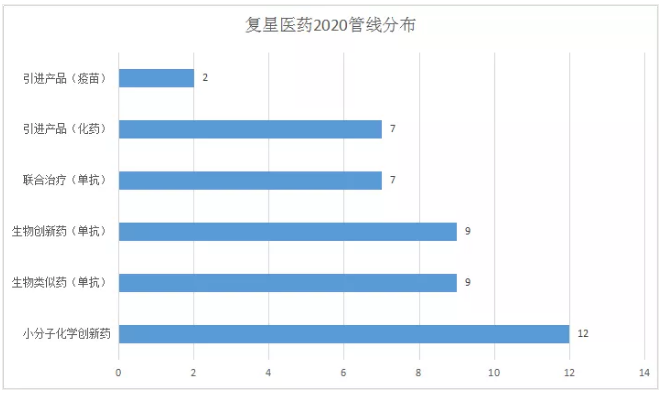
截至2020年6月30日,復星醫藥在研小分子創新藥17項、化學改良型新藥2項、生物創新藥21項、生物類似藥21項、中藥2項、累計引進項目22項(進口創新藥9項,進口仿制藥13項)。
復星醫藥管線分布中單抗類藥物共有25種,其中屬于生物類似藥的有9種,生物創新藥9種,作為聯合治療使用的單抗藥物7種。
上海復星醫藥于2020年3月16日宣布獲BioNTech SE許可在中國獨家開發和商業化基于其專有的mRNA技術平臺研發的針對COVID-19的疫苗產品。并在2021年1月25日上海復星醫藥(集團)股份有限公司與BioNTech SE共同宣布,基于BioNTech的mRNA技術的新冠疫苗COMIRNATY®(即BNT162b2,中文商品名:復必泰TM)獲香港特別行政區食物及衛生局認可在香港作緊急使用。未來供應香港的疫苗將直接由BioNTech在德國的工廠進行生產,用于香港特區政府新冠疫苗接種計劃下的供應、分發和施用等。
 江蘇恒瑞醫藥
在創新藥方面,恒瑞已形成上市一批、臨床一批、開發一批的良性循環,在靶向治療、免疫療法、超長效胰島素等領域的新藥創制已經具備國際領先性。
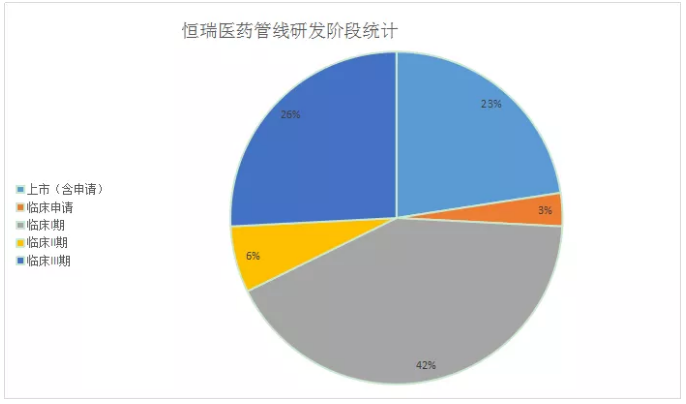
根據恒瑞醫藥官網公布的管線數據,其中共有31條產品線,其中臨床申請1條,進入臨床I期13條,臨床II期2條,臨床III期8條,上市階段7條(1條上市申請中)。
在所有產品線中腫瘤/血液相關14條占45%。2021年2月22日恒瑞醫藥宣布其在研PARP抑制劑(氟唑帕利膠囊)獲得美國FDA國際多中心臨床試驗資格。
 信達生物制藥
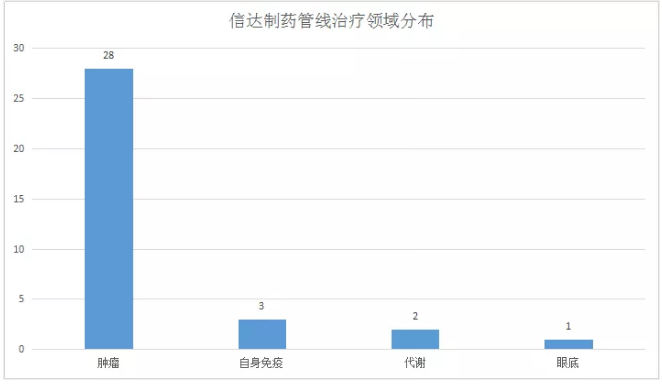
信達生物目前已建立起一條包括23個新藥品種的產品鏈,覆蓋腫瘤、代謝疾病等多個疾病領域。其中4個產品上市,6個品種獲批國家“重大新藥創制”科技重大專項,4個產品進入III期或關性臨床研究,另外還有15個產品已進入臨床研究。
根據信達制藥所發布的管線信息來看,其中屬于血液/腫瘤類藥物多達27種,占總數的79.4%;其中進入上市階段6種,同時還有9種藥物進入臨床III期,可以看到信達制藥的研發方向依舊以抗腫瘤為主。
 百奧泰生物制藥
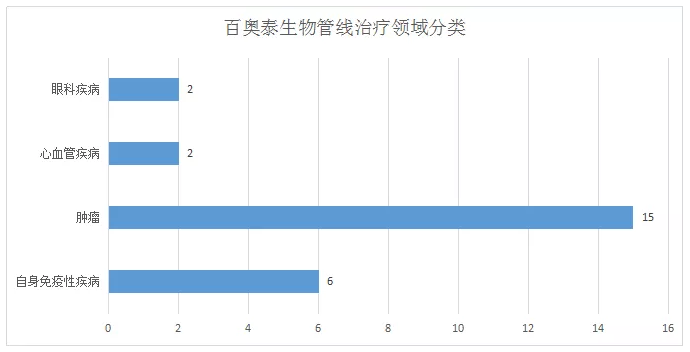
根據百奧泰生物公布的研發管線可以看到其中腫瘤相關藥物15種,自身免疫性疾病藥物6種,心血管疾病藥物2種,眼科疾病藥物2種。
2021年1月28日百奧泰公司宣布美國食品藥品監督管理局(FDA)已受理BAT1706(貝伐珠單抗)注射液的生物制品上市許可申請(BLA)。申請的適應癥包括轉移性結直腸癌、非鱗狀非小細胞肺癌、復發膠質母細胞瘤、轉移性腎細胞癌以及持續性、復發性或轉移性宮頸癌。使得百奧泰公司進軍美國市場更近一步。
 上海君實生物
君實生物是國內首家獲得抗PD-1單克隆抗體NMPA上市批準、抗PCSK9單克隆抗體NMPA臨床申請批準的中國公司,并取得了全球首個治療腫瘤抗BTLA阻斷抗體在中國NMPA和美國FDA的臨床申請批準。
目前具有豐富的在研產品管線,包括19個創新藥,2個生物類似物,主要覆蓋腫瘤、代謝、自身免疫、神經系統、抗感染等重大疾病領域,創新單抗藥重磅品種,包括:用于腫瘤免疫治療的PD-1單抗(JS001),用于高膽固醇血癥治療的PCSK9單抗(JS002)用于腫瘤免疫治療的BTLA單抗(JS004)。其中PD-1單抗拓益(特瑞普利單抗,產品代號:JS001)已完成上市銷售。
 通過對TOP5企業管線的數據統計我們可以看到國內醫藥行業目前研發的重點依舊在抗腫瘤藥物的開發,其中單抗類藥物的開發是重中之重,隨著國內人口老齡化進程的加快,心血管類疾病藥物的開發進度也處于上升的趨勢。隨著國家一系列相關政策的推出,相信國內生物創新藥以及生物類似藥的發展將迎來井噴式的發展。
數據來源:企業官網
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|