
|
|
|||||
|
||||||
百億重磅品種首仿申報上市 市場競爭激烈摘要:
醫藥網4月13日訊
百億市場,首仿將近
近日,CDE官網顯示,先聲藥業的伊布替尼膠囊上市申請正式獲得國家藥監局受理,成為首個在國內遞交上市的伊布替尼仿制藥,有望實現首仿。在國內目前加速首仿藥替代原研,降低藥費的基本背景下,一旦上市想必會對原研的市場有較大沖擊。
伊布替尼是全球第一個上市的BTK抑制劑,由強生和Pharmacyclics(AbbVie子公司)合作開發,于2013年11月獲得FDA批準上市,商品名為“Imbruvica”。截至目前,伊布替尼已在80多個國家和地區獲批。
作為一個高效、高選擇性的小分子抑制劑,伊布替尼適用于既往至少接受過一種治療的慢性淋巴性白血病(CLL)/小淋巴細胞淋巴瘤、套細胞淋巴瘤(MCL)患者的的治療,上市之后銷售額增長迅猛。
據一份針對全球暢銷藥的報告,2014年,上市次年伊布替尼銷售額達到6.92億美元,2015年為14.43億美元,2016年為30.83億美元,2017年為44.46億美元,2018年為62.05億美元,2019年為80.85億美元,2020年為94.42億美元。
在國內市場,伊布替尼的表現同樣亮眼。
2017年強生伊布替尼獲國家藥監局批準在中國上市(商品名為“億珂”,劑型膠囊,規格為140mg),進入醫院市場后銷售額迅速增長,2018年經醫保談判大幅降價后更是快速放量。價格從原來的48600元/盒降為17010元/盒。米內網數據顯示,銷售額從2018年的4442萬增長到2019年5億5717萬,2020年在疫情影響下銷售額依舊漲勢不減,僅上半年就達到6億1582萬元。
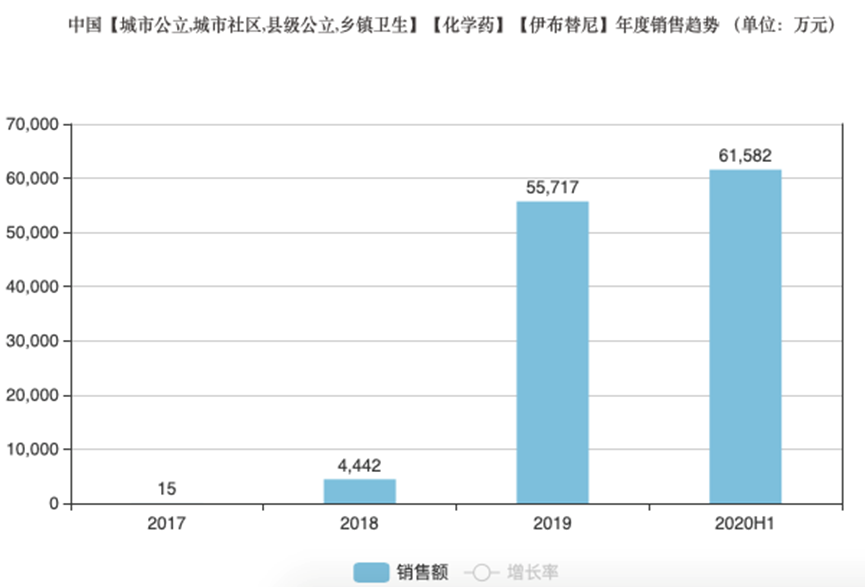 (數據來源:米內網)
市場競爭激烈
BTK是近年來熱門的研究靶點,雖然目前獲批的藥物還不多,但是進入臨床三期試驗的藥物已有一些,且處于臨床二期和一期試驗的藥物非常多,可以預見未來一定會面臨極大的市場競爭。
目前全球已獲批5款BTK抑制劑,分別是強生的伊布替尼、百濟神州的澤布替尼、諾誠健華的奧布替尼、阿斯利康的阿卡替尼以及小野制藥的Tirabrutinib。前三者已在國內獲批上市,其中諾誠健華的奧布替尼和百濟神的澤布替尼均是附條件批準上市。
值得注意的是,雖然市場規模近百億,但市場份額基本由強生伊布替尼獨占,不過新近獲批的藥物,例如2020年上市的澤布替尼、奧布替尼等或因更加優秀的選擇性以及進一步更好的療效和安全性逐漸占領市場,與伊布替尼一較高下。
豐碩創投綜合臨床數據分析,澤布替尼在伊布替尼的基礎上進行了化學結構的優化,擁有更高的 BTK 靶點選擇性和更深的抑制作用,可更大限度減少脫靶。而奧布替尼在此基礎上還顯示出明顯更高的完全緩解率。
除了臨床表現,BTK抑制劑價格方面的競爭同樣激烈。
目前,伊布替尼和澤布替尼均已進入了國家醫保,兩者的協議有效期都是從2021年3月1日至2022年12月31日。澤布替尼的醫保價格為99元(80mg/粒),每月治療費用約為1萬3,相較依布替尼每月1萬7的治療費用更具優勢。
根據Nature reviews Drug Discovery (2021年卷20,期1,頁10)最近發表的文章中預測,2021年伊布替尼的市場可能回落至70億美元左右。
適應癥方面,據豐碩創投梳理,目前BTK適應癥集中在套細胞淋巴瘤、慢性淋巴細胞白血病/小淋巴細胞淋巴瘤等B細胞淋巴瘤亞種,此外,BTK研究的適應癥也已涉及到多種免疫系統疾病,如類風濕性關節炎、系統性紅斑狼瘡、狼瘡腎炎、銀屑病等。
值得注意的是,因為目前BTK發生耐藥的比例相對較低,已經在市場上使用的藥物可以繼續使用較長時間,在激烈的競爭環境下,后續藥物在爭奪相應的腫瘤市場中已有一定難度,更需積極開拓其他適應癥以獲得理想的市場回報。
據了解,目前開發伊布替尼仿制藥的國產廠家多達9家,除了先聲藥業已申報上市外,正大天晴、海正藥業、上海匯倫等已批準臨床,正在開展臨床研究。
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|