
|
|
|||||
|
||||||
抗AD藥迎曙光,哪些企業仍在過評路上?摘要:
醫藥網7月7日訊 日前,美國FDA加速批準了渤健(Biogen)、衛材(Eisai)合作開發的新藥阿杜卡努單抗(Aducanumab,Aduhelm),用于治療阿爾茨海默病(AD)及認知障礙。目前使用的藥物僅能緩解AD癥狀,無法阻止其漸進式發展,而阿杜卡努單抗是首個能夠控制疾病進展的藥物,從而成為這一領域新的里程碑。
國內阿爾茨海默病及認知障礙藥物潛在市場日益增長,2016年國辦發文《國務院辦公廳關于開展仿制藥質量和療效一致性評價的意見》,但五年過去了,抗AD藥僅鹽酸美金剛、鹽酸多奈哌齊、重酒石酸卡巴拉汀等3個品種有企業過一致性評價。
格局
新藥上市匱乏
近日,中國發展基金會發布的《中國發展報告2020:中國人口老齡化的發展趨勢和政策》預測,2022年,中國65歲以上人口將占總人口的14%;到2050年,中國老齡化將達到峰值,65歲以上人口將占總人口的27.9%。
阿爾茨海默病是老齡群體特有的疾病,65歲以上老年人中發病率4%~7%,85歲以上發病率高達20%~30%,嚴重影響了老年人的生活質量。國際阿爾茨海默病協會數據顯示,2019年全球有超過5000萬人患有癡呆癥。在不加干預的情況下,2050年將增加到1.52億,中國目前癡呆癥患者約600萬,每20年將翻一番。
 近30年來,全球獲準上市的AD治療新藥很少。1993年他克林(Tacrine)問世,1996年批準多奈哌齊(Donepezil),2000年批準利斯的明(Rivastigmine),2001年批準加蘭他敏(Galantamine),2003年批準美金剛(Memantine),2014年美金剛多奈哌齊復方制劑(Namzaric)上市。
2020年國內AD市場下滑
2020年,全球阿爾茨海默病藥物市場規模不足50億美元,近5年的復合增長率僅為1.91%。
2019年,我國批準了國家一類新藥甘露特鈉膠囊,與已上市的美金剛、多奈哌齊、卡巴拉汀、加蘭他敏、石杉堿甲等5個藥物構成抗AD市場中流砥柱。
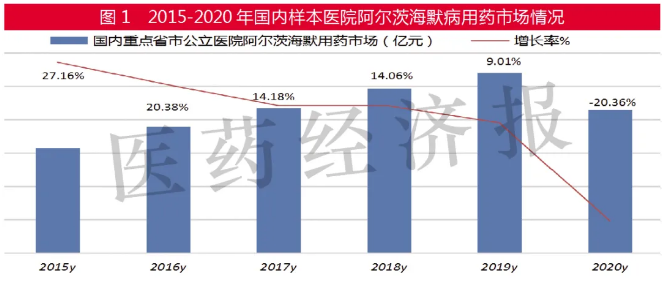
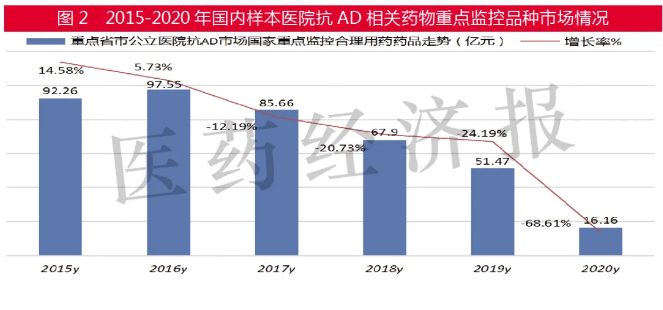
 據米內網數據,2020年國內重點省市公立醫院抗阿爾茨海默病藥物用藥金額近5億元,較上一年下滑20%。在新冠肺炎疫情影響下,門診和住院人數減少;另一方面,國家重點監控用藥合理控費,導致公立醫院用藥總體市場較上一年發生了不小變化。改善記憶及促智藥物總體市場下滑到不足50億元,同比上一年下滑42.28%。
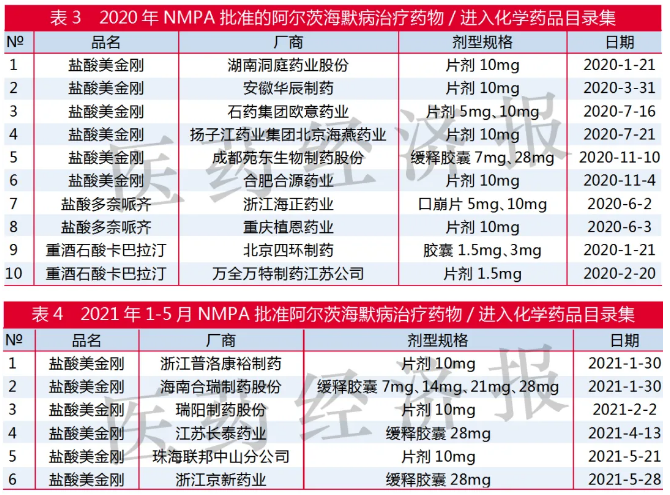
 2020年國家藥監局新批準國內10家藥企生產阿爾茨海默病治療藥物,分別是:鹽酸美金剛、鹽酸多奈哌齊和重酒石酸卡巴拉汀仿制藥,并視同通過一致性評價。2021年1-5月,國家藥監局批準國內5家藥企的鹽酸美金剛仿制藥,并視同通過一致性評價。
 15個藥物逆勢增長
據米內網數據,2019年中國城市公立醫院、縣級公立醫院、城市社區中心以及鄉鎮衛生院神經系統用藥已超過1080億元。2020年國內重點省市公立醫院中,加蘭他敏增長104.47%,雙氫麥角毒堿增長179.86%,吡拉西坦增長101.06%,乙酰谷酰胺增長70.28%,石杉堿甲增長50.75%,卡巴拉汀增長21.28%,尼麥角林增長25.34%,美金剛增長6.80%。高增長率的15個藥物總體平均增長率達到29.51%。
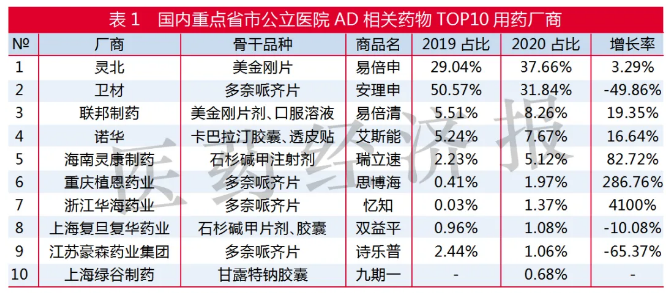
2020年國內重點省市公立醫院阿爾茨海默病相關藥物TOP10用藥廠商是:丹麥靈北、日本衛材、聯邦制藥、瑞士諾華、海南靈康、重慶植恩、浙江華海、上海復旦復華、江蘇豪森和上海綠谷。
 治療藥物
美金剛:靈北易倍申占八成以上
美金剛屬于電壓依賴性、中等程度親和力的非競爭性NMDA受體拮抗劑,是全球第一個治療中、重度阿爾茨海默病的藥物。2003年10月17日,美國FDA批準森林公司的美金剛片,商品名為Namenda,該藥是進入全球暢銷藥500強的唯一一個抗AD藥。2020年全球美金剛及復合制劑銷售額超過5億美元。
國內已批準希臘Pharmanel Commercial Pharmaceutical S.A.的美金剛口服溶液、丹麥靈北(Lundbeck)的美金剛片的注冊,商品名為易倍申。國家藥監局已批準14家國產美金剛口服制劑上市,主要劑型是片劑、口服溶液和緩釋膠囊。13家國內企業的美金剛片通過仿制藥一致性評價。
米內網數據顯示,2020年國內重點省市公立醫院美金剛制劑銷售額為1.99億元,較上年增長6.80%,占據抗AD藥市場46.33%。靈北公司的易倍申占美金剛市場份額80%以上,珠海聯邦制藥的易倍清占據17.83%。2020年湖南洞庭、安徽華辰、白云山總廠、石藥歐意和海達舍畫閣銷售的美金剛制劑進入數據庫,形成了七家競爭局面。美金剛主要在城市公立醫院布局,最近兩年開始加大力度布局縣級公立醫院市場。
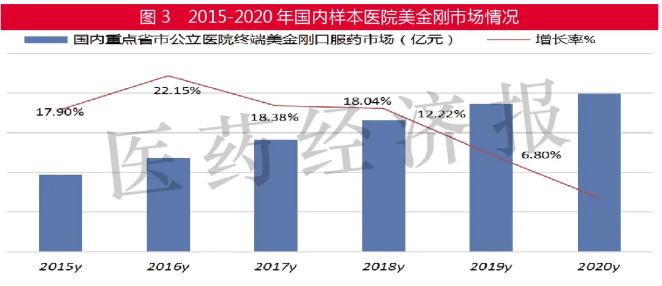 美金剛作用于大腦中的谷酰胺系統,為具有中等親和力的非競爭性的N-甲基-D-天冬氨酸(NMDA)的拮抗劑。2010年,美國FDA批準Forest Labs和Merz制藥的美金剛緩釋膠囊Namenda XR上市;2020年11月,NMPA批準成都苑東生物制藥的美金剛緩釋膠囊在中國首家上市;2021年,海南合瑞制藥、江蘇長泰藥業、浙江京新藥業的美金剛緩釋膠囊獲批。上述產品的上市預計將改變2021年美金剛市場的競爭格局。
多奈哌齊:10億市場3家過評
多奈哌齊是一個具有高度選擇性、可逆性治療阿爾茨海默病的藥物,為第二代中樞性乙酰膽堿酯酶抑制劑,由日本衛材開發,1996年11月獲得美國FDA的特許批準上市,商品名為Aricept,由日本衛材、美國輝瑞聯手進行全球市場的共同開發,具有治療達標劑量小、毒副作用低的特點。全球多奈哌齊市場頂峰期銷售額超過40億美元,專利期滿后銷售額逐年下滑。2019年,衛材的多奈哌齊全球銷售額為3.32億美元。
米內網數據顯示,2019年中國公立醫療機構(城市公立醫院、縣級公立醫院、城市社區中心以及鄉鎮衛生院)終端多奈哌齊用藥金額近10億元,較上年增長17.27%。
截至2020年6月國家藥監局批準海正藥業多奈哌齊口崩片后,已批準17家公司的多奈哌齊口服制劑上市,主要有片劑、膠囊、分散片、口腔崩解片等。
一致性評價方面,衛材(中國)藥業的多奈哌齊片屬于上市藥物目錄集品種,通過一致性評價;2018年10月,華海藥業的多奈哌齊片以仿制藥4類獲準上市,視同通過一致性評價;2019年3月,重慶植恩藥業的“思博海”過評;2020年6月10日,海正藥業的多奈哌齊口崩片以仿制藥4類獲準上市,視同通過一致性評價。目前已經形成進口和國產藥1+3的局面。
據米內網數據,石藥集團歐意藥業的多奈哌齊片以仿制藥4類申報已承辦發件,陜西方舟制藥、江蘇豪森藥業、四川升和藥業、山東羅欣藥業等4家以補充申請處于審評審批階段。
其他藥物:一致性評價還在路上
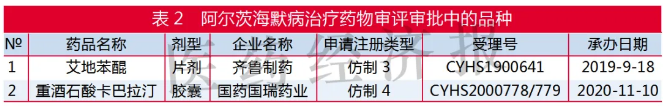
除了前面所述多奈哌齊、美金剛之外,齊魯制藥艾地苯醌仿制3類和國藥國瑞藥業的重酒石酸卡巴拉汀膠囊仿制4類在審評審批中,還有廣東東陽光藥業氫溴酸加蘭他敏口腔崩解片在生物等效性試驗推進中。
輔助類
相關輔助藥物下降69%
2019年國家衛健委公布《第一批國家重點監控合理用藥藥品目錄(化藥及生物制品)》,涉及20個藥物。其中,阿爾茨海默病相關輔助藥物是奧拉西坦、神經節苷脂、腦苷肌肽、依達拉奉、鼠神經生長因子、曲克蘆丁腦蛋白水解物、腦蛋白水解物和長春西汀等8個品種。
數據顯示,國內重點城市公立醫院改善記憶及促智藥物品種從2016年的百億規模下滑到目前的30多億元,2020年同比上一年下降了68.61%。其中:長春西汀下滑最大(-87.52%),其次是曲克蘆丁腦蛋白水解物(-72.95%)、依達拉奉(-70.87%)、奧拉西坦(-70.07%)、鼠神經生長因子(-66.67%)、腦苷肌肽(-66.01%)、腦蛋白水解物(-54.83%)、神經節苷脂(-53.78%)。
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|