
|
|
|||||
|
||||||
恒瑞醫藥97款1類新藥霸屏 31個品種首家過評摘要:
近日,有“創新藥一哥”之稱的恒瑞醫藥動態頻發:SHR8554注射液提交上市申請,HRS-5965片、HR20014注射液、HRS-4642注射液等1類新藥首次獲批臨床。米內網數據顯示,目前恒瑞醫藥有128款創新藥(97款1類新藥)處于申請臨床及以上階段,其中13款(6款1類新藥)已/即將報產,13款(11款1類新藥)處于III期(含II/III期)關鍵臨床。仿制藥方面,60個品種過評(31個為首家),7個品種沖刺首仿(4個獨家報產)。
6大重磅首仿獲批,創新藥大賣超110億
近段時間,恒瑞醫藥接連發布新產品獲批上市的公告:7月2日,其4類仿制藥他克莫司緩釋膠囊獲批生產并視同過評,為國內首仿+首家過評;6月30日,其1類新藥瑞維魯胺片獲批上市,成為國內首個國產新型雄激素受體(AR)抑制劑。
以審評結論日期計,2022年至今,恒瑞醫藥有1款1類新藥首次獲批上市,1款1類新藥新增適應癥;9個品種獲批生產并視同過評,其中有6個為首仿。
2022年至今恒瑞醫藥獲批上市品種
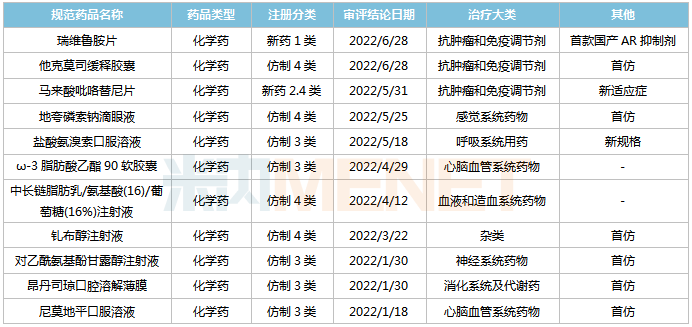 來源:米內網MED2.0中國藥品審評數據庫
6個首仿中,尼莫地平口服溶液、昂丹司瓊口腔溶解薄膜、他克莫司緩釋膠囊、對乙酰氨基酚甘露醇注射液為新劑型。米內網數據顯示,尼莫地平、昂丹司瓊、他克莫司2021年在中國城市公立醫院、縣級公立醫院、城市社區中心以及鄉鎮衛生院(簡稱中國公立醫療機構)終端的銷售規模分別超過7億元、10億元、50億元。
瑞維魯胺片是恒瑞醫藥在國內獲批上市的第11款創新藥(第10款1類新藥),也是首個中國企業自主研發的新型雄激素受體(AR)抑制劑,適用于治療高瘤負荷的轉移性激素敏感性前列腺癌(mHSPC)患者,目前已在北京、上海、廣州、南京、武漢、濟南、長沙、貴陽等多地開出當地首張處方。
米內網數據顯示,恒瑞醫藥2019年及之前獲批的6款創新藥,2021年在中國三大終端6大市場(統計范圍詳見本文末)合計銷售規模超過110億元,其中卡瑞利珠單抗突破40億元,阿帕替尼超過20億元,吡咯替尼、硫培非格司亭接近20億元。
恒瑞醫藥已獲批創新藥
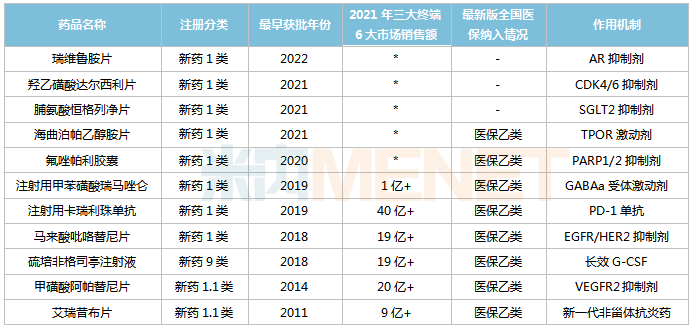 注:未銷售或銷售額低于1億元用*代表
來源:米內網數據庫
11款創新藥中,8款已順利通過談判納入全國醫保目錄,其中阿帕替尼、卡瑞利珠單抗、氟唑帕利、海曲泊帕乙醇胺納入醫保的適應癥達2個及以上。
2022年6月29日,國家醫保局公布《2022年國家基本醫療保險、工傷保險和生育保險藥品目錄調整工作方案》及相關文件,標志著新一輪國家醫保目錄調整工作正式啟動。恒瑞醫藥的瑞維魯胺片、羥乙磺酸達爾西利片、脯氨酸恒格列凈片3款1類新藥有望參與談判。
128款在研新藥霸屏,17個1類新藥上市可期
作為國內“創新藥一哥”,恒瑞醫藥在研創新藥數量遙遙領先。近期,公司研發管線動態頻發:1類新藥SHR8554注射液首次報產,HRS-5965片、HR20014注射液、HRS-4642注射液等1類新藥首次獲批臨床。
自2021年以來,恒瑞醫藥除了堅持自主研發之外,也不斷加強對外合作,先后與基石藥業、天廣實、大連萬春、法國Iktos等企業達成協議。2022年6月,公司斥巨資設立私募投資基金,圍繞醫藥健康產業,特別是生物醫藥領域的創新研發開展投資。有投資者認為,恒瑞醫藥又在加強其BD能力,接下來或許會收購更多生物醫藥公司或新藥等。
米內網數據顯示,含合作引進的新藥在內,恒瑞醫藥有128款創新藥(以藥品名稱計,不含已上市新藥開發新適應癥)在國內處于申請臨床及以上階段,其中有97款為1類新藥。
從研發進展看,13款新藥已/即將申報上市(最高研發進展,下同),其中有6款為1類新藥;13款新藥步入III期(含II/III期)關鍵臨床,其中有11款為1類新藥。
恒瑞醫藥國內在研創新藥
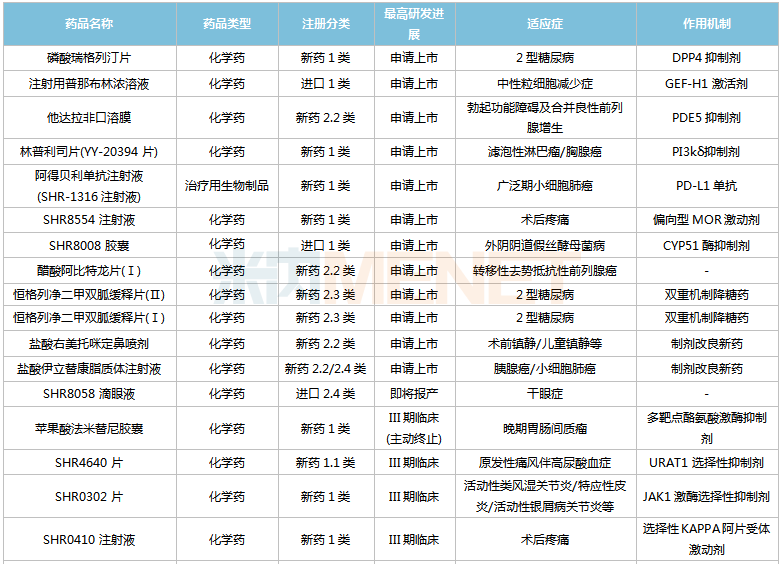 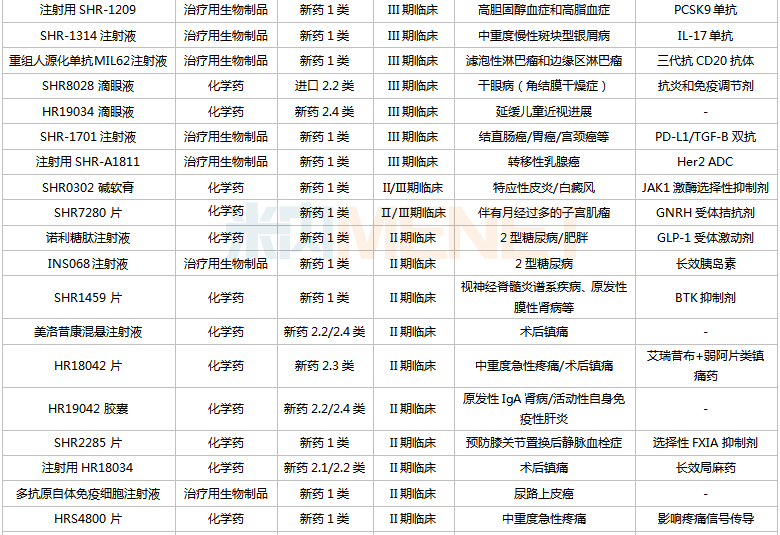 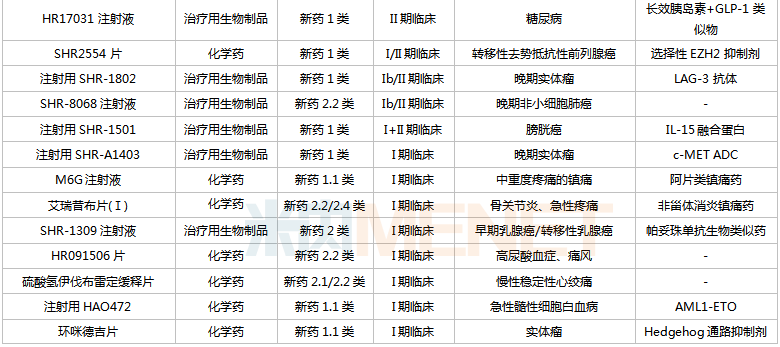 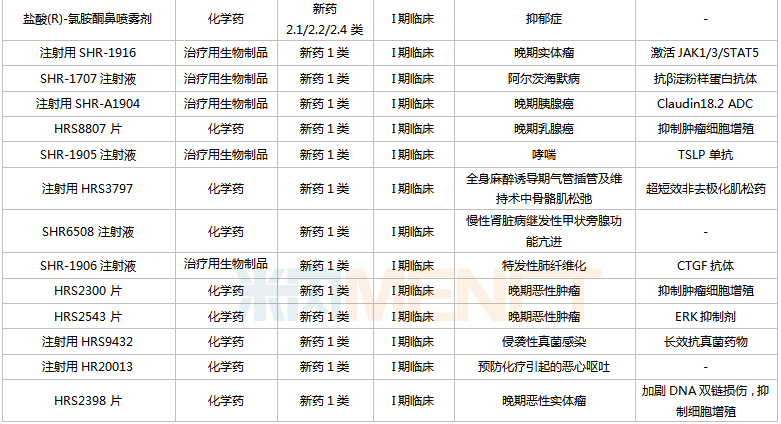 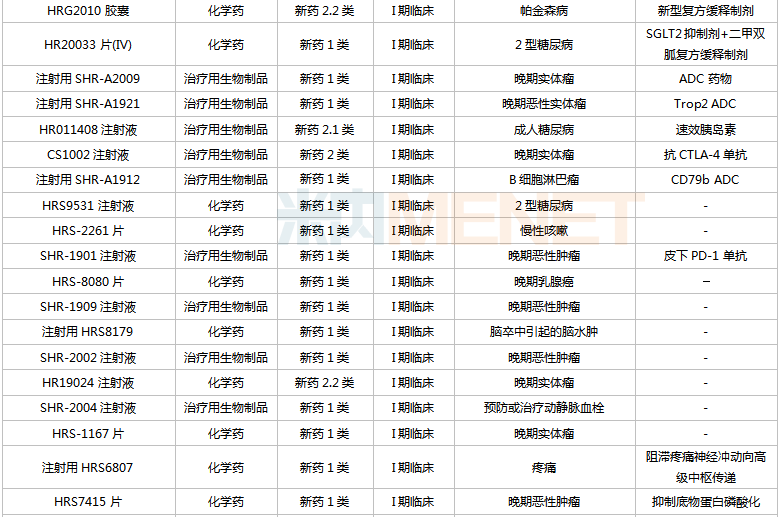 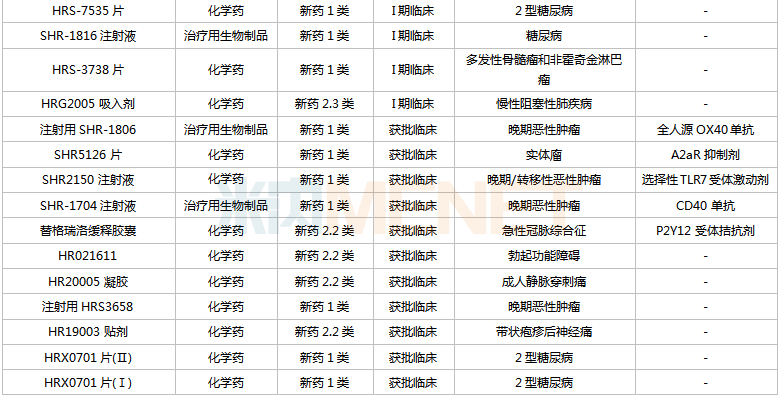 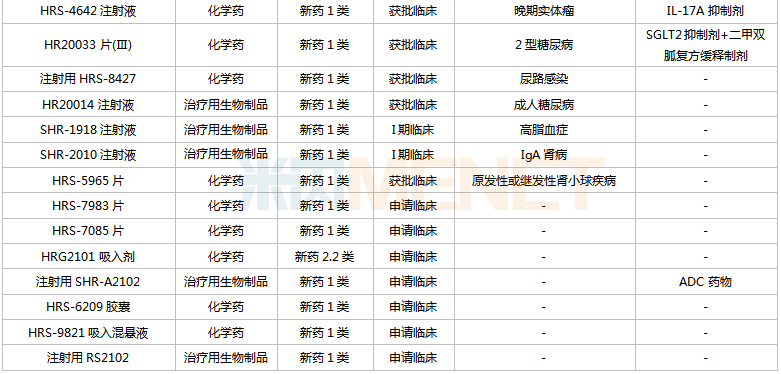 來源:米內網中國藥品臨床試驗公示庫
從適應癥看,恒瑞醫藥在研新藥集中在抗腫瘤和免疫調節劑(腫瘤、自身免疫性疾病)、消化系統及代謝藥(糖尿病、肥胖、止嘔等)、神經系統藥物(疼痛、抑郁癥、帕金森、阿爾茨海默病等)三大治療領域。
抗腫瘤藥占比超4成,涵蓋肺癌、乳腺癌、肝癌、胃癌、前列腺癌、結直腸癌、尿路上皮癌、膀胱癌等多個細分病種;消化系統及代謝藥以糖尿病用藥為主,布局了DPP4、SGLT2、GLP-1等多個熱門靶點,涵蓋小分子口服藥及復方制劑、速效胰島素、長效胰島素等;神經系統藥物以麻醉止痛藥為主,其中1類新藥SHR8554(偏向型MOR激動劑)、2類改良型新藥鹽酸右美托咪定鼻噴劑已報產。
在靶點方面,恒瑞醫藥布局全球熱門靶點和前沿工藝,如PD-(L)1、BTK、CDK4/6、ADC、JAK、CD20等;在CD40(TNFRSF5)、CD47、IL-15、OX40(TNFRSF4)、CTGF、RORC(RZRG)、ROMK、TIM-3、GPR40(FFAR1)等暫無藥物獲批的靶點上也有布局。
在PD-(L)1靶點上,恒瑞醫藥的卡瑞利珠單抗已獲批上市,目前已成為納入醫保適應癥最多的國產PD-1單抗,且還在持續開展聯合用藥及拓寬新適應癥的臨床研究。此外,PD-L1單抗阿得貝利單抗已報產,PD-L1/TGF-B雙抗SHR-1701步入III期臨床,皮下注射PD-1單抗SHR-1901步入了I期臨床。
恒瑞醫藥是目前在研ADC藥物最多的國內藥企,有8款新藥處于申請臨床及以上階段,其中靶向Her2的ADC藥物SHR-A1811進展最快,目前正在開展III期臨床。此外,有6款ADC藥物步入I期臨床,1款ADC藥物正在申報臨床。
60個品種過評,7個品種搶首仿
7月26日,國家藥監局官網顯示,恒瑞醫藥的碘化油注射液(罌粟乙碘油注射液)通過一致性評價,為國內首家。
目前恒瑞醫藥有60個品種過評(31個為首家),涵蓋12個治療大類,集中在抗腫瘤和免疫調節劑(13個品種)、神經系統藥物(11個品種)、心血管系統藥物(8個品種)等治療領域;劑型分布較廣,除了普通口服常釋劑型,還包括注射劑、緩控釋制劑、吸入劑、滴眼劑、口溶膜等。
恒瑞醫藥過評情況
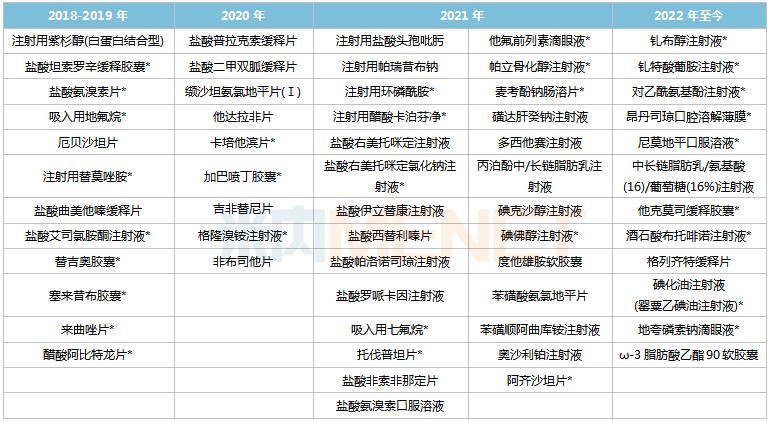 注:帶*為首家/獨家過評
來源:米內網MED2.0中國藥品審評數據庫
在政策陣痛面前,恒瑞醫藥決定“砍掉”部分仿制藥項目,只做創新藥和有核心價值的高端仿制藥。2022年至今,公司僅提交了3個品種的一致性評價補充申請,暫無仿制藥提交上市申請。
目前恒瑞醫藥有8個一致性評價補充申請品種在審,其中注射用奧沙利鉑、碳酸氫鈉林格注射液、復方醋酸鈉林格注射液(鈉鉀鎂鈣葡萄糖注射液)、美司鈉注射液、羅格列酮片等品種暫無企業過評。新分類申報仿制藥中(不含已撤回或不批準品種),有7個暫無首仿(含劑型首仿)獲批。
恒瑞醫藥新分類申報且暫無首仿獲批的品種
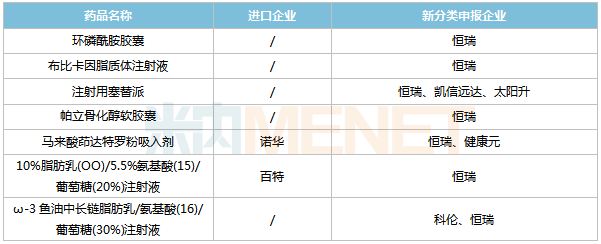 來源:米內網MED2.0中國藥品審評數據庫
環磷酰胺膠囊、布比卡因脂質體注射液、帕立骨化醇軟膠囊、10%脂肪乳(OO)/5.5%氨基酸(15)/葡萄糖(20%)注射液由恒瑞醫藥獨家申報。
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|